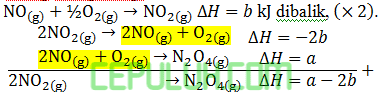(1). Soal Jawaban Perubahan Entalpi Diketahui Kalor Jenis
Soal Jawaban 1 Perubahan Entalpi Diketahui Kalor Jenis
Apabila 50 ml larutan NaOH 1M direaksikan dengan 50 ml larutan HCl 1M dalam bejana, ternyata suhularutan naik dari 29℃ menjadi 33℃. Jika Kalor jenis produk c=4,2J/(gram℃), maka perubahan entalpi reaksi:
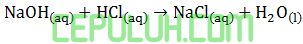
adalah….
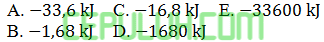
Jawaban: B Pembahasan:
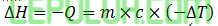
Anggap massa jenis larutan sama dengan air (ρ=1 g/ml) sehingga besar massa sama dengan volumenya.
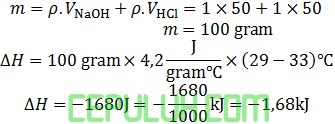
(2). Termokimia @ Kalor Jenis
15. Campuran CaO (Ar Ca = 40, O = 16) dan H2O (kalor jenis spesifik = 4 J·g-1·°K-1) berlebih memberikan reaksi:
CaO(s) + H2O(ℓ) ➔ Ca(OH)2(s) ΔH =-64 kJ
Bila panas yang dihasilkan reaksi ini mampu menaikkan suhu 100 gram air sebesar 0,1 K maka jumlah CaO yang bereaksi adalah …
A. 0,035 g D. 0,350 g
B. 0,080 g E. 3,500 g
C. 0,105 g
15. Pembahasan:
CaO(s) + H2O(ℓ) ➔ Ca(OH)2(s)
ΔH = -64 kJ /1 mol CaO
ΔH untuk menaikkan suhu 100 gram air sebesar 0,1 K = -m ·c·ΔT
= -100·4·0,1 = -40 J = -0,04 kJ.
mol CaO yang bereaksi= (0,04/64)·l mol = 6,25·10-4mol
massa CaO yang bereaksi = 6,25·10-4·56 = 0, 035 gram
Jawaban: A
(3). Soal Jawaban 3 Perubahan Entalpi Diketahui Kalor Jenis
Sebanyak 50 ml HCl 1M direaksikan dengan 50 ml NaOH 1M. Setelah bereaksi suhu larutan berubah dari 27℃ menjadi 33,5℃. Jika massa jenis larutan1 g/ml dan kalor jenis larutan 4,18 J/(g.℃) maka harga ∆H reaksi adalah ….kJ/mol.
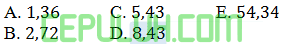
Jawaban: B Pembahasan:
Anggap massa jenis larutan sama dengan air (ρ=1 g/ml) sehingga besar massa sama dengan volumenya.
(4). Efisiensi Kalor Proses Pemanasan Etanol
13. Sebanyak 500 ml air dipanaskan dengan menggunakan lampu spirtus. Jika jumlah etanol yang terbakar 2 g, ternyata suhu air naik sebesar 5,14°C. Efisiensi kalor pada proses pemanasan tersebut adalah …
(ΔHf C2H5 = -227 kJ/mol; CO2(g) = -393,5 kJ/mol; H2O(g) = -242 kJ/mol; kalor jenis air = 4,18 J·g-1·°K-1; Ar H = 1, C = 12, O = 16)
A. 1% B. 2% C. 10% D. 20% E. 40%
13. Pembahasan:
Penentuan ΔH secara kalorimetri:
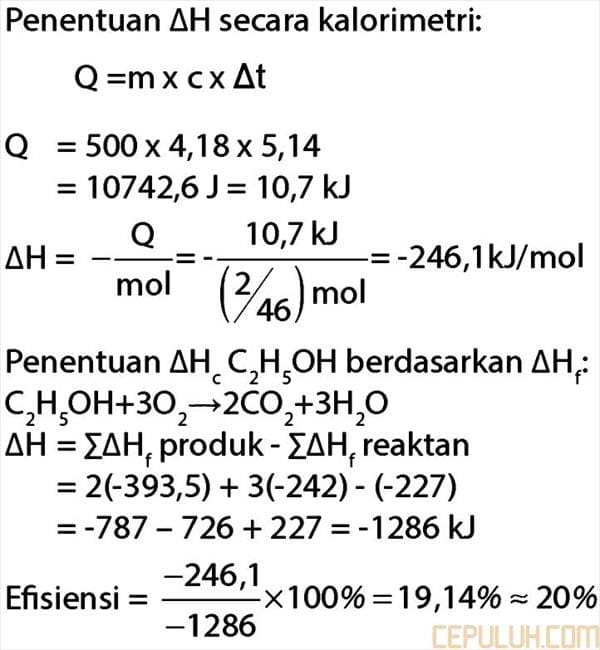
Jawaban: D
(5). Soal Jawaban 2 Perubahan Entalpi Diketahui Kalor Jenis
A. 1,6 B. 2,4 C. 4 D. 12 E. 8
Jawaban: B Pembahasan:
Kita hitung mol metana:
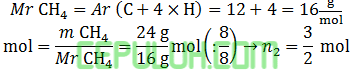
Menghitung kalor dengan perbandingan:
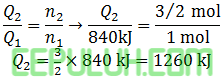
Persen kalor menjadi kalor untuk memanaskan air:
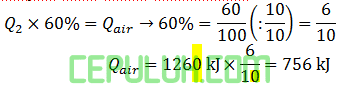
Kalor untuk memanaskan air sampai mendidih 100℃.
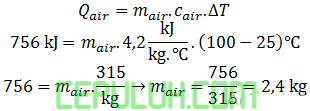
(6). Soal Jawaban 4 Perubahan Entalpi Diketahui Kalor Jenis
Jumlah kalor yang digunakan untuk menaikkan suhu 100 gram air dari 30℃ sampai mendidih adalah ….kJ. (kalor jenis air 4,18 J/(g.K))
Jawaban: B Pembahasan:
Suhu air mendidih 100℃. Beda suhu di skala Celsius sama dengan di Kelvin.
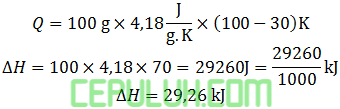
Termokimia # Entalpi Pembakaran Standar
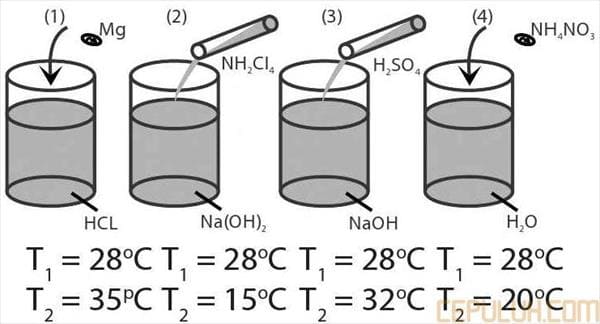
Termokimia # Reaksi Eksoterm Endoterm
Termokimia # Entalpi Pembentukan Standar
Termokimia # Entalpi Tiga Persamaan Reaksi
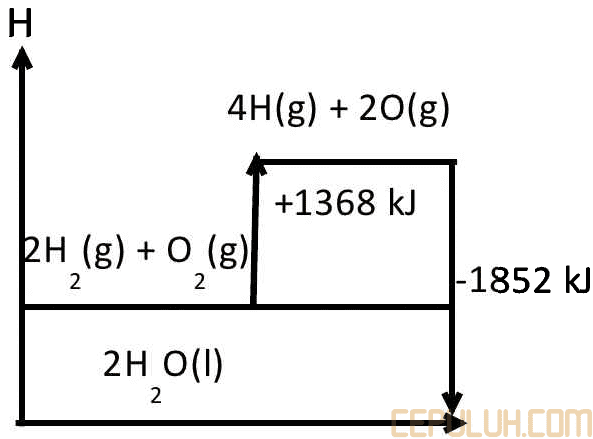
Termokimia # Bagan Gambar Grafik Diagram
Termokimia # Perubahan Entalpi
Termokimia # Entalpi Pembakaran
Termokimia # Energi Ikatan Rata-rata
Termokimia # Kalorimeter Kalor Jenis