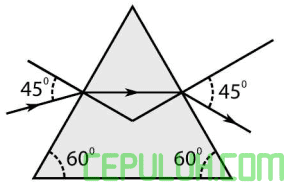
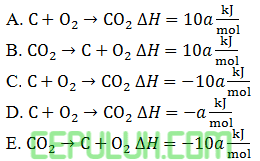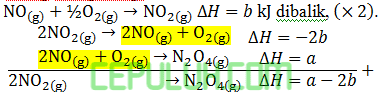(1). Soal Perubahan 2 Entalpi Pembakaran Standar
Jika kalor pembentukan:

maka perbandingan antara kalor pembakaran sempurna gas propana dgn kalor pembakaran tidak sempurna dalam kJ/mol adalah ….
B. 1111∶2749 E. 2746∶2222
C. 2046∶1197
Jawaban: C Pembahasan:
Zat yang dibakar ada di kiri sebagai reaktan.
Pembakaran sempurna hidrokarbon oleh molekul oksigen menghasilkan karbondioksida dan air.

Setarakan banyak atom di kiri dan di kanan panah agar sama.

Pembakaran tidak sempurna hidrokarbon oleh molekul oksigen menghasilkan karbonmonoksida dan air.

Setarakan banyak atom di kiri dan di kanan panah agar sama.

Carilah masing-masing ∆H pembakaran 1 mol propana.

Pembakaran sempurna:

Pembakaran tidak sempurna:

(2). Soal Jawaban Perubahan Entalpi Pembakaran Standar
Perhatikan persamaan reaksi kimia berikut:

Pernyataan yang benar ….
A. perubahan entalpi pembentukan C2H2= -2600kJ/mol
B. perubahan entalpi pembakaran C2H2= -2600kJ/mol
C. perubahan entalpi pembentukan C2H2= -1300kJ/mol
D. perubahan entalpi pembakaran C2H2= -1300kJ/mol
E. perubahan entalpi pembentukan CO2 & H2O= -1300 kJ/mol
Jawaban: B Pembahasan:
Adanya molekul oksigen O2 di sebelah kiri panah artinya perubahan entalpi pembakaran.
Perubahan entalpi pembakaran C2H2= -2600 kJ/mol (yang ini).
Jika perubahan entalpi pembakaran standarnya dihitung maka koefisien C2H2 harus sama dengan satu. Persamaan reaksi dikali ½:

(3). Soal Perubahan 3 Entalpi Pembakaran Standar
Persamaan termokimia yang benar untuk pembakaran karbon, jika diketahui kalor yang diperlukan untuk penguraian 4,4 gram karbondioksida menjadi karbon dan oksigen adalah a kJ. (Ar.C=12,O=16) ….

Jawaban: B Pembahasan:
Hitunglah mol karbondioksida.

Kalor diperlukan dimasukkan endoterm (+), dibebaskan dikeluarkan eksoterm (-).
Penguraian karbondioksida 1/10 mol butuh kalor Q=a kJ
Penguraian CO2 1 mol=1/10 mol×10 butuh kalor Q=10a kJ
Zat yang diuraikan ada di kiri sebagai reaktan. Jadi,

(4). Soal Perubahan 4 Entalpi Pembakaran Standar
Bila 0,126 gram karbon monoksida dibakar dan panas yang dilepas sebesar 1.260 J maka panas pembakaran gas CO sebesar ….kJ/mol.(Ar.C=12,O=16)
B. 28 D. 226,8
Jawab: B Pembahasan:

Kalor dilepas/dikeluarkan ∆H=(-):
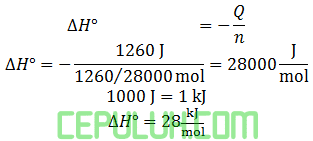
A. –185 B. –101 C. 101 D. 143 E. 185
Jawaban: C Pembahasan:
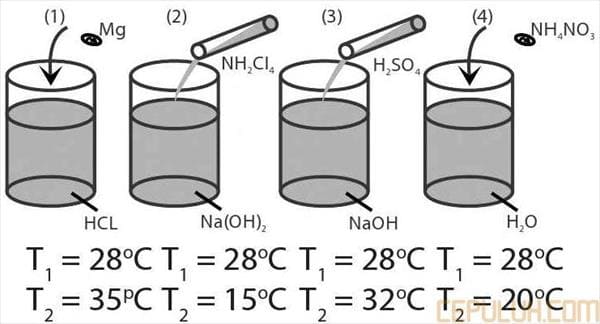
Perubahan energi dalam ∆U, kalor Q kerja W. ke-1.com
+Q sistem menerima (menyerap) kalor
–Q sistem membebaskan kalor
+W sistem menerima kerja
–W sistem melakukan kerja
(5). Entalpi Pembentukan Entalpi Pembakaran Propana
17. Diketahui entalpi pembentukan dari:
ΔHf°C3H8(g) = -103,9 kJ/mol
ΔHf°CO2(g) = -393,5 kJ/mol
ΔHf° H2O(g) = -242,0 kJ/mol
Jika 22 gram C3H8 (ArC = 12, H = 1) dibakar sempurna maka entalpi pembakaran propana tersebut adalah …
A. -255,1 kJ D. -2044,6 kJ
B. -511,2 kJ E. -6193,1 kJ
C. -1022,3 kJ
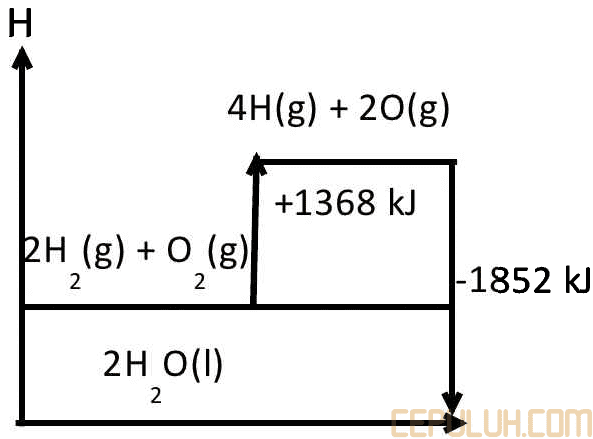
17. Pembahasan:
Data dari entalpi pembentukan standar bisa digunakan untuk menghitung ΔH reaksi (ΔHf.

Jawaban: C
Termokimia # Reaksi Eksoterm Endoterm
Termokimia # Entalpi Pembentukan Standar
Termokimia # Entalpi Tiga Persamaan Reaksi
Termokimia # Bagan Gambar Grafik Diagram
Termokimia # Perubahan Entalpi
Termokimia # Entalpi Pembakaran
Termokimia # Energi Ikatan Rata-rata
Termokimia # Entalpi Pembakaran Standar