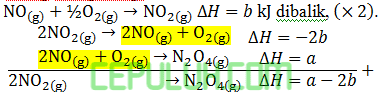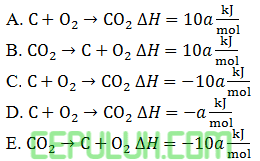(1). Perubahan Entalpi Pembakaran
Diketahui ∆Hf beberapa senyawa adalah sebagai berikut:

Tentukan ∆H reaksi pembakaran:
A. 1 mol gas karbon monoksida (CO)
B. 4,48 liter gas propana (C3H8) pada STP
Pembahasan:
A. Gas oksigen O2(g) digunakan untuk membakar. Satu mol artinya bilangan di depan CO(g) satu.

Volum 1 mol gas STP sebanyak 22,4 liter

Pembakaran sempurna hidrokarbon oleh molekul oksigen menghasilkan karbondioksida dan air.

Setarakan banyak atom di kiri dan di kanan panah agar sama.

Carilah ∆Hc°, pembakaran 1 mol propana.

(2). Entalpi Pembakaran Etena
11. Reaksi:
2C2H2(g) + 5O2(g) ➔ 4CO2(g) + 2H2O(ℓ) ΔH = -2600 kJ.
dari reaksi ini pernyataan yang benar adalah …
(1) Terjadi pelepasan kalor
(2) Perubahan entalpi pembakaran 1 mol etena -1300 kJ
(3) 1 mol etena dibakar akan melepaskan 2 mol CO2
(4) Reaksi pembakaran etena adalah endoterm
11. Pembahasan:
Reaksi:
2C2H2(g) + 5O2(g) ➔ 4CO2(g) + 2H2O(ℓ) ΔH = -2600 kJ
(1) Reaksi di atas memiliki ΔH negatif yang artinya terjadi pelepasan/pembebasan kalor.
(2) Reaksi tersebut merupakan perubahan entalpi pembakaran 2 mol etena maka perubahan entalpi pembakaran 1 mol etena sebesar-1300 kJ.
C2H2(g) + 5/2O2(g) ➔ 2CO2(g) + H2O(ℓ) ΔH = -1300 kJ
(3) Pembakaran 1 mol etena akan melepaskan 2 mol CO2.
(4) Reaksi pembakaran etena adalah eksoterm (ΔH negatif).
Pilihan (1), (2), dan (3) benar.
Jawaban: A
(3). Entalpi Pembakaran Gas Asetilena
3. Gas asetilena (C2H2) yang mempunyai entalpi pembakaran -320 kkal/mol dapat dibuat menurut reaksi:
CaC2(s) + 2H2O ➔ Ca(OH)2(aq) + C2H2(g)
Jika dalam suatu proses digunakan 160 gram CaC2 dan diasumsikan yang dapat bereaksi hanya 80 % maka untuk pembakaran gas asetilena yang terbentuk akan dihasilkan kalor sebesar … (ArC = 12; Ca = 40)
A. 320 kkal/mol D. 800 kkal/mol
B. 480 kkal/mol E. 960 kkal/mol
C. 640 kkal/mol
3. Pembahasan:
CaC2(s) + 2H2O ➔ Ca(OH)2(aq) + C2H2(g)
mol CaC2 yang bereaksi adalah:

Jadi, untuk pembakaran 2 mol gas C2H2 dihasilkan kalor sebesar 640 kkal.
Jawaban: C
(4). Kalor Pembakaran Etanol Kalor Reaksi Fermentasi Glukosa Kalor Pembakaran Glukosa
19. Jika diketahui kalor pembakaran etanol (C2H5OH) adalah -1380 kJ/mol dan kalor reaksi fermentasi glukosa C6H12O6 ➔ 2C2H5OH + 2CO2 adalah -60 kJ/mol maka kalor pembakaran glukosa (C6H12O6) adalah …
A. -1440 kJ/mol D. 2880 kJ/mol
B. -2760 kJ/mol E. 2940 kJ/mol
C. -2820 kJ/mol
19. Pembahasan:
untuk menentukan pembakaran glukosa menurut persamaan berikut:

Jawaban: C
(5). Entalpi Pembakaran Bahan Bakar Energi Paling Besar
6. Tabel berikut menyajikan data entalpi pembakaran untuk lima jenis bahan bakar.
| Bahan Bakar | ΔH(kJ/mol) | Mr |
| Hidrogen | -287 | 2 |
| Metana | -803 | 16 |
| Propana | -2201 | 44 |
| Isobutana | -2868 | 58 |
| Neopentana | -3515 | 72 |
Pembakaran 1 gram bahan bakar yang menghasilkan energi paling besar adalah …
A. hidrogen D. isobutana
B. metana E. neopentana
C. propana
6. Pembahasan:

Jawaban: A
(6). Persamaan Temokimia Kalor Pembakaran Etuna dari Metanol
33. Perhatikan persamaan temokimia berikut.
2C2H2(g) + 5O2(g) ➔ 4CO2(g) + 2H2O(g) ΔH = -2600 kJ
CO(g) + 2H2(g) ➔ 2CH3OH(g) ΔH = -130 kJ
Jika kalor pembakaran etuna digunakan untuk menghasilkan gas H2 dari metanol maka massa etuna yang diperoleh untuk menghasilkan 32 g H2 adalah … g
A. 10,4 B. 20,8 C. 41,6 D. 83,2 E. 166,4
33. Pembahasan:
Energi yang diperlukan untuk mengubah metanol menjadi H2

Jawaban: B
(7). Dua Reaksi Termokimia Pembakaran Grafit CaCO CaCO3
22. Pehatikan dua reaksi termokimia berikut
C(grafit) + O2(g) ➔ CO2(g) ΔH = -432 kJ/mol
CaO(s) + CO2(g) CaCO3(s) ΔH = -180 kJ/mol
Bila panas yang dihasilkan dari pembakaran grafit digunakan untuk membuat CaO dari CaCO3 maka massa grafit yang diperlukan untuk menghasilkan 5,6 kg CaO adalah … kg
A. 0,5 B. 1,8 C. 2,0 D. 4,0 E. 6,0
22. Pembahasan:
Panas energi yang diperlukan untuk memanaskan CaCO3 menjadi CaO = 100 mol·180 kJ/mol = 18.000 kJ

Jawaban: A
(8). Perubahan Entalpi Pembakaran
Soal Pembahasan 1 Perubahan Entalpi Pembakaran
Jika diketahui persamaan termokimia

maka kalor yang diserap untuk membakar 44,8 liter N2 saat STP (0℃,1 atm) adalah … kJ.

Jawab: D Pembahasan:
volume gas saat STP 22,4 liter/mol, mol N2:

Koefisien, bilangan di depan senyawa adalah jumlah mol.

(9). Entalpi Pembakaran Gas Asetilena Proses Pengelasan
21. Gas asetilena yang digunakan pada proses pengelasan adalah:
CaC2(s) + 2H2O(ℓ) ➔ Ca(OH)2(aq) + C2H2(g)
Entalpi pembakaran C2H2 adalah -320 kkal/mol. Kalor yang dihasilkan dari pembakaran gas C2H2 yang diperoleh dari 96 g CaC2adalah … kkal
A. 960 B. 800 C. 640 D. 480 E. 320
21. Pembahasan:
Entalpi Pembakaran
ΔH reaksi 1 mol suatu zat dengan gas O2

Jawaban: D
(10). Perubahan Entalpi Pembakaran
Pernyataan yang benar untuk reaksi:

adalah ….
A. Kalor pembentukan CO=2x kJ/mol
B. Kalor penguraian CO=x kJ/mol
C. Kalor pembakaran CO=2x kJ/mol
D. Kalor pembakaran CO=½x kJ/mol
E. Kalor pembentukan CO=½x kJ/mol
Jawab: D Pembahasan:
Ini adalah persamaan reaksi:
(1). Pembakaran 2 mol karbon monoksida CO(g),
(2). Pembentukan 2 mol karbon dioksida CO2(g).
Satuan kJ/mol artinya persamaan mesti standar 1 mol.

Termokimia # Energi Ikatan Rata-rata
Termokimia # Entalpi Pembakaran