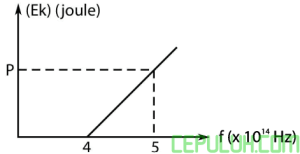
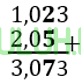(1). Reaksi Penetralan Asam Kuat Basa Kuat
Jika 100 ml larutan asam klorida dengan pH=2 dicampurkan pada 100 ml larutan natrium hidroksida dengan pH=10 akan diperoleh larutan dengan ….
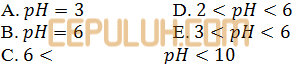
Jawab: D Pembahasan:
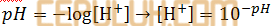
Khusus asam kuat monovalen berlaku M=[H+], contoh HCl
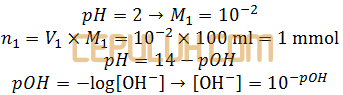
Khusus basa kuat monovalen berlaku M=[OH–], contoh NaOH
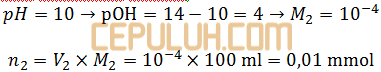
Asam kuat dan basa kuat bereaksi sampai salah satunya habis. Itu menghasilkan garam netral dan air, pH ditentukan konsentrasi sisa asam atau basa.
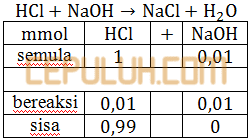
Penambahan sedikit mol NaOH tidak banyak bereaksi 0,99≅1 malah menjadikan HCl lebih encer.
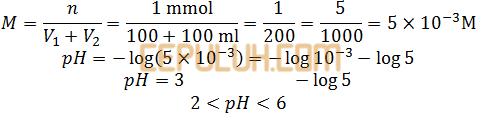
(2). Reaksi Penetralan Asam Kuat Basa Kuat
Asam sulfat sebanyak 20 ml dititrasi dengan larutan NaOH 0,1 M ternyata diperlukan 30 ml larutan NaOH maka konsentrasi asam sulfat adalah ….M.
Titrasi berbeda dengan penetralan, Titrasi menyembabkan senyawa habis bereaksi meskipun campuran pH≠7 bukan netral.
Asam sulfat mol H2SO4=20 ml×M2=20V2.
Basa mol NaOH=30 ml×0,1 M=3 mmol.

mmol H2SO4 semula dikurangi bereaksi sama dengan nol.
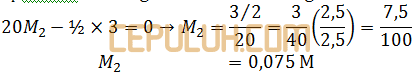
(3). Reaksi Penetralan Asam Kuat Basa Kuat
Sebanyak 0,4 gram NaOH dilarutkan ke dalam air, larutan yang terjadi akan dapat ss larutan HCl 0,1 M sebanyak ….ml. (Ar Na=23,O=16,H=1)
Jawab: D Pembahasan:
Reaksi penetralan menyebabkan kedua senyawa asam-basa kuat habis tak bersisa.
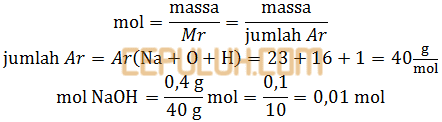
Asam mol HCl =0,1 M×V2=0,1V2.
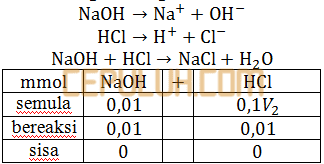
mmol H2SO4 semula dikurangi bereaksi sama dengan nol.
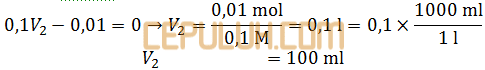
(4). Reaksi Penetralan Asam Kuat Basa Kuat
Jika 50 ml larutan HNO3 0,4 M tepat dinetralkan oleh 200 ml larutan Ba(OH)2 maka konsentrasi larutan Ba(OH)2 adalah ….M.
Jawab: D Pembahasan:
Reaksi penetralan menyebabkan kedua senyawa asam-basa kuat habis tak bersisa.
Asam mol HNO3=50 ml×0,4 M=20 mmol.
Basa mol Ba(OH)2=200 ml×M2=200M2.

mmol Ba(OH)2 semula dikurangi bereaksi sama dengan nol.
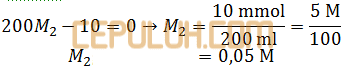
(5). Reaksi Penetralan Asam Kuat Basa Kuat
Sebanyak 200 ml larutan NaOH mempunyai pH=13. Volume larutan HCl 0,1M yang harus direaksikan dengannya agar menjadi campuran pH=2 adalah …ml.
Jawab: D pembahasan:
Larutan NaOH:
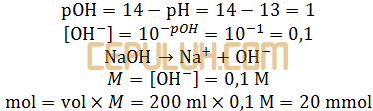
Larutan HCl:
Konsentrasi campuran:
Berarti bersifat asam, zat yang tersisa adalah asam kuat HCl, basa kuat habis bereaksi, garam netral dihasilkan.
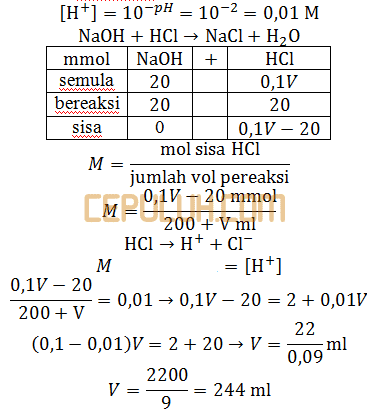
(6). Reaksi Penetralan Asam Kuat Basa Kuat
untuk menetralkan 100 ml larutan KOH 0,1 M diperlukan larutan H2SO4 0,1 M sebanyak ….ml.
Jawab: B Pembahasan:
Reaksi penetralan menyebabkan kedua senyawa asam-basa kuat habis tak bersisa.
Basa mol KOH=100 ml×0,1 M=10 mmol.
Asam mol H2SO4=0,1 M×V2=0,1V2.
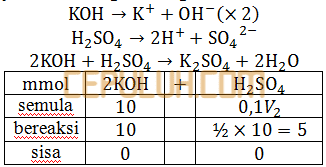
mmol H2SO4 semula dikurangi bereaksi sama dengan nol.
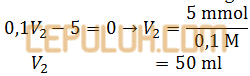
(7). Reaksi Penetralan Asam Kuat Basa Kuat
Asam sulfat H2SO4 sebanyak 20 ml dinetralkan oleh larutan NaOH 0,1M. Bila ternyata diperlukan 30 ml larutan NaOH maka kemolaran larutan asam sulfat tersebut adalah ….M.
Jawab: A pembahasan:
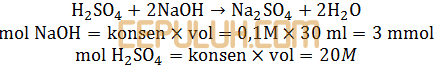
Perbandingan mol bereaksi sama dengan perbandingan koefisien, di sini 1∶2. Jadi mol asam sulfat yang bereaksi setengah kali natrium hidroksida.
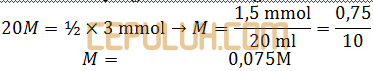
(8). Massa Molekul Relatif Asam Organik untuk Menetralkan NaOH
18. Sampel asam organik 0,25 g dilarutkan dalam 50 ml NaOH 0,1 M. untuk menetralkan NaOH yang tidak digunakan oleh sampel asam organik memerlukan 25 ml HCl 0,01 M. Massa molekul relatif sampel asam organik tersebut adalah …
A. 52,6 B. 100 C. 150 D. 200 E. 300
18. Pembahasan:

Jawaban: A
(9). Kumpulan Soal Reaksi Penetralan Asam Kuat Basa Kuat
Soal Pembahasan 1 Reaksi Penetralan Asam Kuat Basa Kuat
Pasangan senyawa di bawah ini yang larutannya dalam air terionisasi sempurna adalah ….
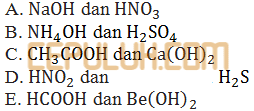
Terionisasi sempurna adalah sifat garam netral hasil reaksi asam kuat dengan basa kuat.
Asam kuat di antaranya asam nitrat HNO3, asam sulfat H2SO4.
Basa kuat di antaranya hidroksi alkali NaOH, alkali tanah Ca(OH)2, Be(OH)2.
(10). Agar Larutan AgNO Menjadi Netral Maka Diperlukan NaOH
2. untuk mengendapkan semua logam Ag dari 15 ml larutan AgNO3 0,1 M ditambahkan 20 ml HCl 0,2 M. Agar larutan menjadi netral maka diperlukan NaOH 0,1 M sebanyak … ml
A. 12,5 B. 25 C. 50 D. 15 E. 30
2. Pembahasan:
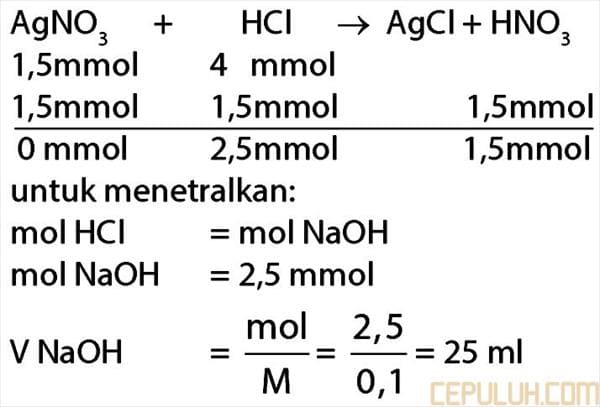
Jawaban: B
Larutan Asam-Basa # Warna Indikator Trayek pH
Larutan Asam-Basa # Titrasi Asam Basa
Larutan Asam-Basa # Bronsted Lowry Konjugasi Donor Akseptor
Larutan Penyangga Buffer # Sisa Basa Lemah dan Garamnya
Larutan Penyangga Buffer Sisa Asam Lemah dan Garamnya
Sisa Asam Basa Lemah dan Garamnya
Stoikiometri # Perbandingan Volume
Larutan Asam-Basa # Penetralan Kuat