(1). Perbandingan Waktu Laju Reaksi Diketahui Perubahan Konsentrasi
Perhatikan data eksperimen sebagai berikut:
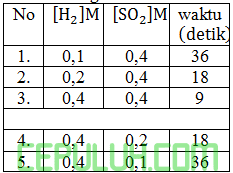
Berdasarkan data tersebut, pernyataan yang benar adalah ….
A. Orde reaksi terhadap H2 adalah 2
B. Orde reaksi terhadap SO2 adalah 2
C. Orde reaksi total adalah 4
D. Persamaan laju reaksi v=k[H2]2[SO2]2
E. Laju reaksi menjadi 4 kali jika[H2] dan [SO2] diperbesar 2 kali
Jawab: E Pembahasan:
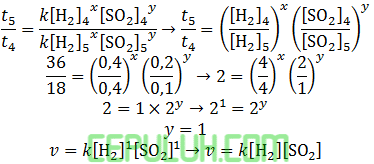
waktu (t) berbanding terbalik dari laju.
untuk mencari orde [H2], pilih konsentrasi [SO2] sama. Pilih reaksi no 1 dan 2.
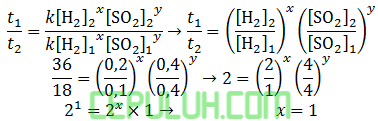
untuk mencari orde [SO2], pilih konsentrasi [H2] sama. Pilih reaksi no 4 dan 5.
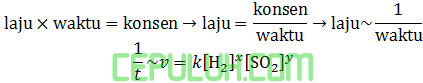
Orde reaksi total x+y=1+1=2.
Jika konsentrasi kedua [H2] dan [SO2] (×2). Pilih reaksi no satu:
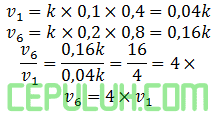
(2). Lama Waktu Reaksi Kimia
Laju reaksi 2A(aq)+B2(aq)→C(s)+D(aq). Ditentukan dengan mengukur waktu yang diperlukan untuk membentuk sejumlah endapan C.
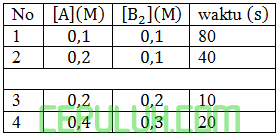
Waktu yang dibutuhkan jika konsentrasi pereaksi A 0,6 M dan konsentrasi pereaksi B2 adalah 0,3 M adalah ….
A. 1,5 B. 15 C. 150 D. 0,15 E. 0,015
Jawab: A Pembahasan:
waktu (t) berbanding terbalik dari laju.
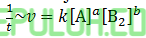
untuk mencari orde [A], pilih konsentrasi [B2] sama. Pilih reaksi 2 dan 1.
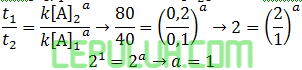
untuk mencari orde [B2], pilih konsentrasi [A] sama. Pilih reaksi 3 dan 2.
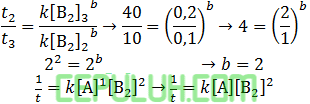
Masukan data yang mudah, pilih no 1 untuk menghitung tetapan k:
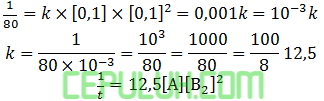
Jika [A]=0,6M dan [B2]=0,3M maka waktu reaksi:
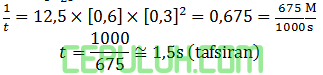
(3). Orde Waktu Reaksi
Data percobaan pengukuran laju reaksi diperoleh data sebagai berikut:
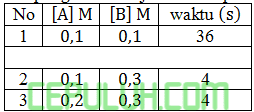
dari data tersebut dapat disimpulkan bahwa orde reaksi total adalah ….
A. 0 B. 1 C. 2 D. 3 E. -2
Jawab: C Pembahasan:
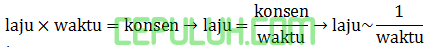
waktu (t) berbanding terbalik dari laju.
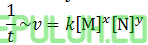
untuk mencari orde [A], pilih konsentrasi [B] sama. Pilih reaksi 3 dan 2.
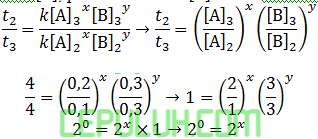
Orde [A] sama dengan x=0.
untuk mencari orde [B], pilih konsentrasi [A] sama. Pilih reaksi 2 dan 1.
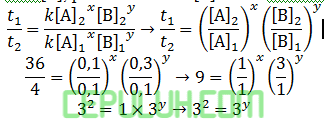
orde [B] sama dengan y=2
orde reaksi totalnya x+y=0+2=2.
(4). Orde Waktu Reaksi
Reaksi antara M+N→O+P memberi data sebagai berikut:
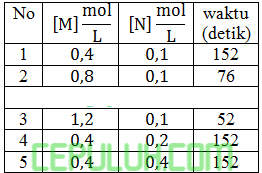
Orde reaksi total adalah ….
A. 3 B. 2 C. 1 D. ½ E. 0
Jawab: C Pembahasan:
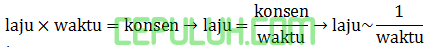
waktu (t) berbanding terbalik dari laju.
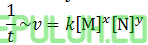
untuk mencari orde [M], pilih konsentrasi [N] sama. Pilih reaksi 2 dan 1.
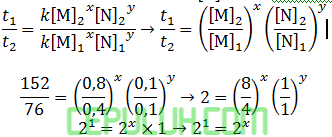
Orde reaksi [M] sama dengan x=1.
untuk mencari orde [N], pilih konsentrasi [M] sama. Pilih reaksi 4 dan 1.
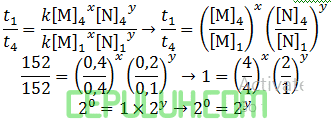
Orde reaksi [N] sama dengan y=0
Orde reaksi totalnya x+y=1+0=1.
(5). Perbandingan Waktu Laju Reaksi Diketahui Perubahan Konsentrasi
Reaksi kimia:
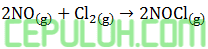
mempunyai persamaan laju v=k[NO]2[Cl2]. Apabila pada suhu tetap konsentrasi NO diperkecil 2 kali, sedangkan konsentrasi Cl2 tetap, maka laju reaksinya ….
A. lebih besar 4 kali
B. lebih kecil 4 kali
C. sama seperti semula
D. lebih kecil 2 kali
E. lebih besar 2 kali
Jawab: B Pembahasan:
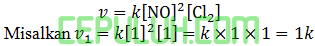
Setelah [NO] diperkecil 2 kali atau (×½) dan [Cl2] tetap:
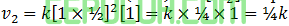
Perbandingan:
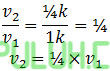
Laju reaksi menjadi lebih kecil 4 kali.
(6). Perbandingan Waktu Laju Reaksi Perubahan Konsentrasi
Soal Pembahasan 1 Perbandingan Waktu Laju Reaksi Diketahui Perubahan Konsentrasi
Suatu reaksi ditulis dengan persamaan v=k[X]2[Y]. Jika masing-masing konsentrasi pereaksi diperbesar 3 kali, maka laju reaksi menjadi ….kali.
A. 6 B.3 C. 27 D. 9 E. 18
Jawab: C Pembahasan:
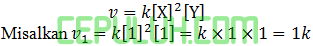
Setelah [X] diperbesar (×3) dan [Cl2] diperbesar (×3):
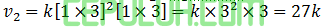
Perbandingan:
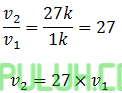
Laju reaksi menjadi 27 kali.
(7). Perbandingan Waktu Laju Reaksi Diketahui Perubahan Konsentrasi
Reaksi antara NO(g) dan O2(g) berorde dua terhadap konsentrasi NO dan berorde satu terhadap konsentrasi O2. Jika konsentrasi semua pereaksi dinaikkan menjadi tiga kali konsentrasi semula, maka laju reaksinya bila dibandingkan dengan laju mula-mula adalah ….
Jawab: D Pembahasan:
Orde adalah pangkatnya konsentrasi.
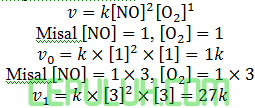
Perbandingan:
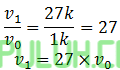
(8). Perbandingan Waktu Laju Reaksi Diketahui Perubahan Konsentrasi
Suatu reaksi
mempunyai persamaan kecepatan v=k[P][Q]2. Jika konsentrasi P dinaikkan 2 kali dan Q dinaikkan menjadi tiga kalinya, maka laju reaksi nya adalah…
Jawab: E Pembahasan:
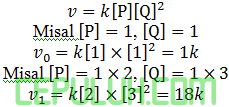
Perbandingan:
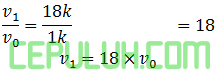
(9). Lama Waktu Reaksi Kimia
Soal Pembahasan 1 Menghitung Lama Waktu Reaksi Kimia
dari hasil percobaan reaksi A+2B→AB2 mempunyai persamaan laju reaksi v=k[A][B]2. pada konsentrasi awal [A]=0,1M dan [B]=0,1M, reaksi berlangsung 96 detik. Maka jika percobaan dilakukan pada konsentrasi awal [A]=0,3M dan konsentrasi awal [B]=0,2M, reaksi akan berlangsung dalam … detik.
A. 576 B. 384 C. 24 D. 6
Jawab: D Pembahasan:

waktu berbanding terbalik dari laju.

(10). Kecepatan Reaksi NO Menit
25. Diketahui reaksi: 2NO(g) + Cl2(g) ➔ 2NOCl(g), dan kecepatan reaksinya pada 130°C dapat dirumuskan dengan persamaan v = 0,4 (NO)2(Cl2) dalam satuan M/menit Apabila 2 mol gas NO dan 2 mol gas Cl2 dalam volume 4 liter direaksikan pada 130°C maka setelah 80% mol gas NO bereaksi kecepatan reaksinya saat itu adalah … M/menit
A. 0,0004 B. 0,0012 C. 0,0048 D. 0,0256 E. 0,0004
25. Pembahasan:

Jawaban: B
Rumus Persamaan Laju Reaksi
Laju Reaksi # Laju Kecepatan
Kesetimbangan Kimia # Pergeseran Kesetimbangan
Elektrokimia # Elektrolisis Faraday Endapan Arus Listrik
Laju Reaksi # Lama Waktu Reaksi









