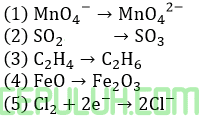(1). Hukum Proust Perbandingan Massa Tetap Massa Besi dan Oksigen
16. Data reaksi oksidasi besi sebagai berikut:
| No | Massa Fe (gram) | Massa O (gram) | Massa Fe2O3 (gram) | Massa zat tersisa |
|---|---|---|---|---|
| 1. | 1,40 | 0,60 | 2,00 | – |
| 2. | 2,30 | 0,90 | 3,00 | 0,2 gram Fe |
| 3. | 2,45 | 1,05 | 3,50 | – |
| 4. | 3,50 | 1,50 | 5,00 | – |
Perbadingan massa besi dan oksigen dalam senyawa yang terbentuk adalah …
A. 5:2 B. 5:3 C. 7:2 D. 7:3 E. 7:5
16. Pembahasan:
Hukum Perbandingan Massa Tetap (Hukum Proust):
Hukum Proust: Perbandingan massa unsur dalam senyawa adalah tertentu dan tetap.
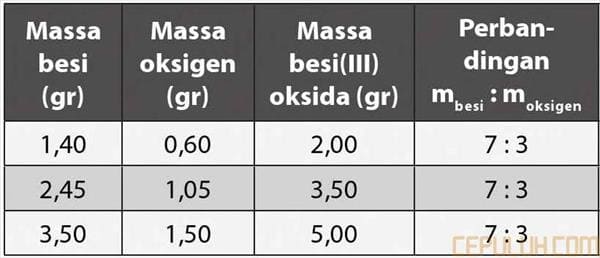
Perbandingan massa besi dan besi dalam senyawa yang terbentuk adalah 7 : 3.
Jawaban: D
(2). Stoikiometri @ Perbandingan Massa Unsur-unsur dalam 1 Senyawa
18. Data yang diperoleh pada percobaan reaksi antara Cu dan S membentuk CuS sebagai berikut:
| Percobaan | Massa Cu (gr) | Massa S (gr) | Massa CuS (gr) |
|---|---|---|---|
| 1 | 4 | 2 | 6 |
| 2 | 6 | 2 | 6 |
| 3 | 8 | 4 | 12 |
| 4 | 8 | 10 | 12 |
Berdasarkan data percobaan tersebut maka perbandingan massa unsur Cu dengan S dalam senyawa CuS adalah …
A. 4:5 B. 3:1 C. 2:1 D. 1 :3 E. 1 :2
18. Pembahasan:
Tembaga dapat bereaksi dengan belerang membentuk tembaga(II) sulfida dengan perbandingan sebagai berikut:
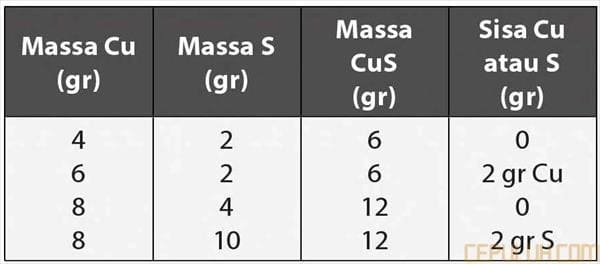
Berdasarkan data tersebut, perbandingan massa Cu dengan S dalam tembaga(ll) sulfida hasil reaksi adalah 4:2 = 2: 1.
Jawaban: C
(3). Stoikiometri @ Perbandingan Massa Unsur-unsur dalam 1 Senyawa
17. Perhatikan tabel percobaan reaksi pembentukan gas CO2 dari karbon dan oksigen berikut ini!
| Massa C (gram) | Massa O (gram) | Massa CO2 (gram) |
|---|---|---|
| 1,5 | 4 | 5,5 |
| 3,0 | 8 | 11,0 |
| 4,0 | 8 | 11,0 |
| 5,0 | 12 | 16,5 |
Berdasarkan tabel perbandingan massa C dan O dalam senyawa CO2 adalah …
A. 1 : 3 B. 1 : 4 C. 3 : 1 D. 3 : 8 E. 4 : 1
17. Pembahasan:
Hukum Proust: Perbandingan massa unsur dalam senyawa adalah tertentu dan tetap.
Perbandingan massa C dan O dalam senyawa CO2 adalah 3:8.
Jawaban: D
(4). Asetilena Bahan Bakar Nyala Las Reaksi Kalsium Karbida dan Air Kalsium Karbida
16. Asetilena digunakan sebagai bahan bakar dalam nyala las dapat dihasilkan dari reaksi antara kalsium karbida dan air. Berapa gram asetilena akan dibentuk dari 0,5 mol kalsium karbida?
(Diketahui Ar H = 1, C = 12, O = 16, dan Ca = 40)
A. 13 g B. 15 g C. 20 g D. 26 g E. 39 g
16. Pembahasan:
Perbandingan koefisien = perbandingan mol
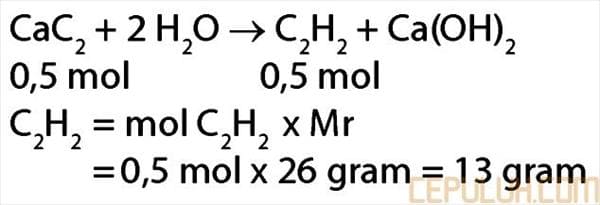
Jawaban: A
(5). Nitrogen Dioksida Hujan Asam Menghasilkan Asam Nitrat
22. Di stratosfer, nitrogen dioksida bereaksi dengan air untuk menghasilkan NO dan asam nitrat yang berperan dalam hujan asam, reaksi dengan H2O adalah
3NO2(g) + H2O(ℓ) ➔ 2HNO3(aq) + NO(g)
Satu mol NO2 akan menghasilkan asam nitrat (Mr = 63) sebanyak …
A. 21 g B. 42 g C. 63 g D. 93 g E. 126 g
22. Pembahasan:
Perbandingan koefisien = perbandingan mol
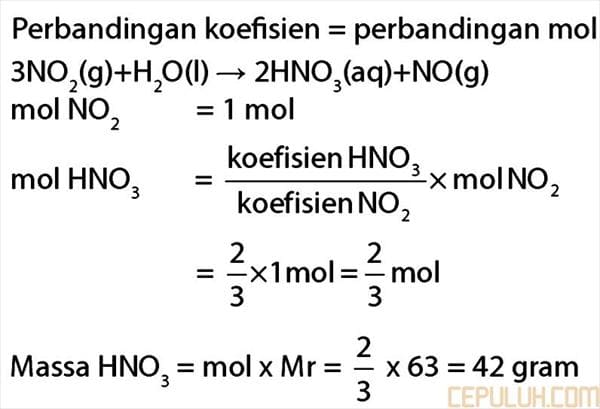
Jawaban: B
(6). Jumlah Logam Vanadium Pentoksida dengan Kalsium
20. Logam vanadium dihasilkan dengan cara mereaksikan vanadium pentoksida dengan kalsium pada suhu tinggi. Reaksi yang terjadi (belum setara):
Jika 91 g V2O5 (Mr = 182) bereaksi dengan 120 g Ca (Ar = 40) maka jumlah logam vanadium (Ar = 51) yang dihasilkan adalah …
A. 25,5 g B. 51,0 g C. 76,5 g D. 102,0 g E. 122,5 g
20. Pembahasan:

Jawaban: B
(7). Kobalt Klorida Hidrat
37. Kobalt klorida adalah garam anorganik yang berwarna biru, sedangkan hidratnya, CoCl2.xH2O berwarna mentega (merah). Sebanyak 1,19 g CoCl2.xH2O dilarutkan dalam air sampai volume 50 ml. Kemudian, ke dalam 25 ml larutan ini dimasukkan larutan AgNO3 berlebih sehingga terbentuk endapan AgCl sebanyak 0,7175 g. dengan demikian, nilai x adalah …
(Ar Co = 59; Cl = 35,5; H = 1; O = 16; Ag = 108; N = 14)
A. 2 B. 3 C. 4 D. 6 E. 19
37. Pembahasan:

Jawaban: D
(8). pada Temperatur dan Tekanan Standar Butuh Paduan Sebanyak Gram
21. Sebuah paduan (aliansi) yang terdiri atas 90% Al (Ar = 27) dan 10% Cu (Ar = 63,5) digunakan untuk menghasilkan gas H2 dengan cara mereaksikan dengan asam klorida. untuk menghasilkan 6,72 liter gas H2, pada temperatur dan tekanan standar maka dibutuhkan paduan sebanyak … gram
A. 5,4 B. 6,0 C. 6,6 D. 7,6 E. 8,0
21. Pembahasan:

Jawaban: B
(9). Oksidasi Ch4 Sempurna Menjadi CO2 Gram CO2 Terbentuk
23. Suatu campuran gas terdiri atas 8 g gas metana, (CH4) dan 8 g oksigen. Jika seandainya semua oksigen yang ada digunakan untuk mengoksidasi CH4 dengan sempurna menjadi CO2, berapa gram CO2 yang terbentuk? (H = 1, C = 12, O = 16)
A. 4,0 g B. 5,5 g C. 8,0 g D. 11,0 g E. 22,0 g
23. Pembahasan:
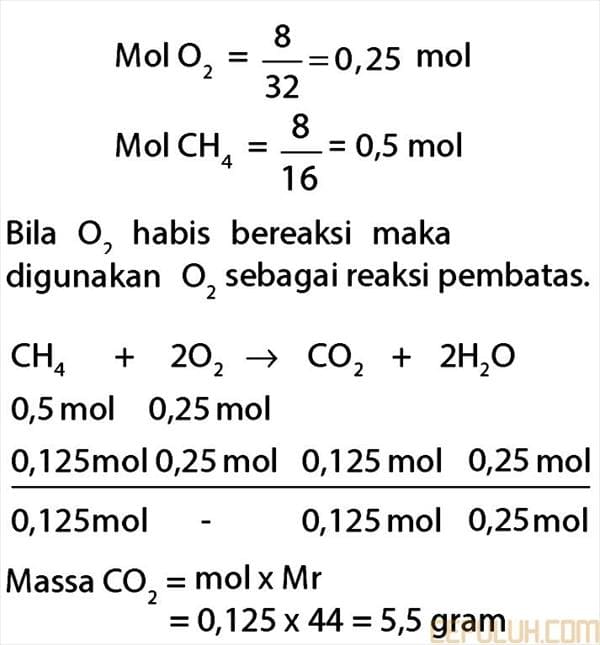
Jawaban: B
(10). Reduksi Besi III Oksida dengan CO Menghasilkan Besi Reaksi
11. Reduksi besi (III) oksida dengan CO menghasilkan besi menurut persamaan reaksi:
Fe2O3 + 3CO ➔ 2Fe + 3CO2
untuk menghasilkan 11,2 kg besi (Ar Fe = 56) dibutuhkan besi (III) oksida (Mr Fe2O3 = 160) sejumlah …
A. 22 kg B. 20 kg C. 18 kg D. 16 kg E. 15 kg
11. Pembahasan:
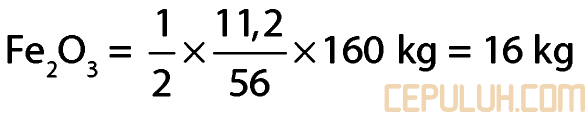
Jawaban: D
Stoikiometri # Perbandingan Massa