(1). Soal Bentuk Molekul Hibridisasi Senyawa IF5 Segiempat Piramida
Soal bentuk molekul senyawa IF5 (nomor atom I=53,e lektron valensi atom I=7; nomor atom F=9, elektron valensi atom F=7)
Jawaban: segiempat piramida sesuai AX5E.
Pembahasan:
Konfigurasi elektron atom I: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p5, elektron valensi 7.
Konfigurasi elektron atom F: 1s2 2s2 2p5, elektron valensi 7.
Bentuk molekul senyawa IF5 menurut teori VSEPR
Struktur Lewis:

Atom I sebagai atom pusat memiliki 7 elektron valensi, lima elektron valensi terlibat dalam ikatan dengan lima atom F di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=5) maka atom I memiliki satu pasangan elektron bebas (PEB=1) sehingga IF5 diprediksi berbentuk segiempat piramida AX5E.

Bentuk molekul senyawa IF5 menurut teori hibridisasi
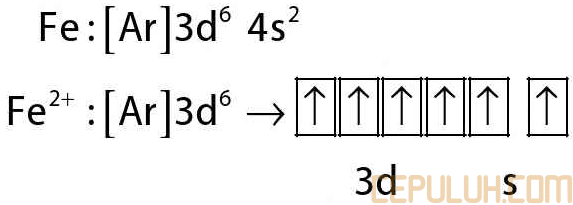
Diagram orbital atom I:

Dalam molekul IF5, satu atom I mengikat 5 atom F. Pengikatan ini dapat berlangsung dengan mengeksitasi 2 elektron dari orbital 5p ke orbital 5d.

Kemudian 5 elektron dari 5 atom F memasuki orbital 5p dan 5d sehingga terbentuk orbital hibrida sp3d2. Bentuknya bukan oktahedral, tetapi berbentuk segiempat piramida. Hal ini disebabkan satu dari orbital sp3 d2 digunakan untuk menampung satu pasang elektron bebas dari atom I.

Jadi, molekul IF5 diprediksi berbentuk segiempat piramida.
(2). Soal Bentuk Molekul Senyawa BrF5 Segiempat Piramida
Soal bentuk molekul senyawa BrF5 (nomor atom Br=35, elektron valensi atom Br=7; nomor atom F=9, elektron valensi atom F=7)
Jawaban: segiempat piramida sesuai AX5E.
Pembahasan:
Konfigurasi elektron atom Br: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5, elektron valensi 7.
Konfigurasi elektron atom F: 1s2 2s2 2p5, elektron valensi 7.
Bentuk molekul senyawa BrF5 menurut teori VSEPR
Struktur Lewis:

Atom Br sebagai atom pusat memiliki 7 elektron valensi, lima elektron valensi terlibat dalam ikatan dengan lima atom F di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=5) maka atom Br memiliki satu pasangan elektron bebas (PEB=1) sehingga BrF5 diprediksi berbentuk segiempat piramida sesuai AX5E.

Bentuk molekul senyawa BrF5 menurut teori hibridisasi
Diagram orbital atom Br:

Dalam molekul BrF5, satu atom Br mengikat 5 atom F. Pengikatan ini dapat berlangsung dengan mengeksitasi 2 elektron dari orbital 4p ke orbital 4d.

Kemudian 5 elektron dari 5 atom F memasuki orbital 4p dan 4d sehingga terbentuk orbital hibrida sp3 d2. Bentuknya bukan oktahedral, tetapi berbentuk segiempat bipiramida. Hal ini disebabkan, satu dari orbital sp3 d2 digunakan untuk menampung satu pasang elektron bebas dari atom Br.

Jadi, molekul BrF5 diprediksi berbentuk segiempat bipiramida.
(3). Soal Bentuk Molekul Senyawa PF3 Segitiga Piramida
Soal bentuk molekul senyawa PF3 (nomor atom P=15, elektron valensi atom P=5; nomor atom F=9, elektron valensi atom F=7)
Jawaban: segitiga piramida AX3E.
Pembahasan:
Konfigurasi elektron atom P: 1s2 2s2 2p6 3s2 3p3, elektron valensi 5.
Konfigurasi elektron atom F: 1s2 2s2 2p5, elektron valensi 7.
Bentuk molekul senyawa PF3 menurut teori VSEPR
Struktur Lewis:

Atom P sebagai atom pusat memiliki 5 elektron valensi, tiga elektron valensi terlibat dalam ikatan dengan tiga atom F di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=3) maka atom P memiliki satu pasangan elektron bebas (PEB=1) sehingga PF3 diprediksi berbentuk segitiga piramida sesuai AX3E.

Bentuk molekul senyawa PF3 menurut teori hibridisasi
Diagram orbital atom P:

Dalam molekul PF3, satu atom P mengikat 3 atom F. Kemudian 3 elektron dari 3 atom F memasuki orbital 3p sehingga terbentuk orbital hibrida sp3. Bentuknya bukan tetrahedral, tetapi berbentuk segitiga piramida. Hal ini disebabkan satu dari orbital sp3 digunakan untuk menampung satu pasang elektron bebas dari atom P.

Jadi, molekul PF3 diprediksi berbentuk segitiga piramida.
Bentuk Molekul Oktahedral
Bentuk Molekul Tetrahedral Terdistorsi
Bentuk Molekul Segitiga Datar
Bentuk Molekul Linear
Bentuk Molekul Segitiga Piramida
Bentuk Molekul Tetrahedral
Bentuk Molekul Segiempat Piramida