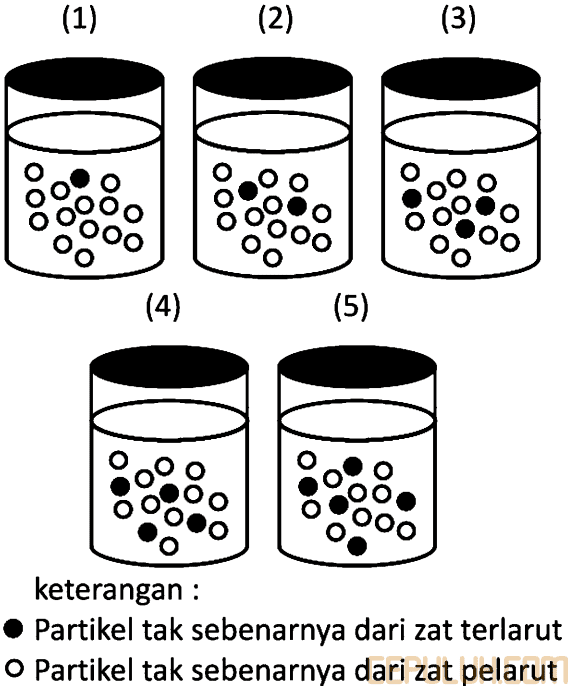
(1). Memisahkan Air dan Alkohol Berdasarkan Titik Didihnya
Anwar ingin memisahkan air dan alkohol dalam suatu larutan. Dalam hal ini Anwar ingin memisahkan air dan alkohol berdasarkan titik didihnya. Cara yang tepat untuk memisahkan air dan alkohol adalah ….
A. filtrasi C. kromatografi
B. dekatansi D. destilasi
Jawab: D Bahas:
Filtrasi (disebut pula sebagai Penyaringan) adalah pembersihan partikel padat dari suatu fluida dengan melewatkannya pada medium penyaringan, atau septum, yang di atasnya padatan akan terendapkan. Rentang filtrasi pada industri mulai dari penyaringan sederhana hingga pemisahan yang kompleks.
Dekatasi adalah sebuah proses yang dilakukan untuk memisahkan campuran larutan dan padatan yang paling sederhana yaitu dengan menuangkan cairan secara perlahan sehingga endapan tertinggal dibagian dasar bejana.
Kromatografi adalah suatu teknik pemisahan molekul berdasarkan perbedaan pola pergerakan antara fase gerak dan fase diam untuk memisahkan komponen (berupa molekul) yang berada pada larutan. Molekul yang terlarut dalam fase gerak, akan melewati kolom yang merupakan fase diam.
(2). Larutan Terlarut Pelarut Titik Didih Paling Rendah
81. Perhatikan tabel di bawah ini!
| Larutan | Terlarut | Pelarut |
|---|---|---|
| P | 0,10 mol | 1 kg |
| Q | 0,20 mol | 1 kg |
| R | 0,30 mol | 1 kg |
| S | 0,40 mol | 1 kg |
| T | 0,50 mol | 1 kg |
Larutan yang mempunyai titik didih paling rendah adalah …
A. larutan P D. larutan S
B. larutan Q E. larutanT
C. larutan R
81. Pembahasan:
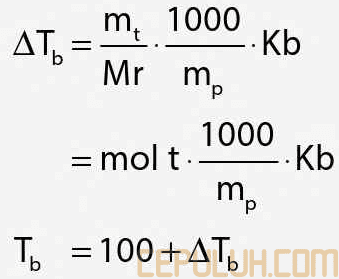
Persamaan di atas menunjukkan rendah mol zat terlarut, semakin didih larutan akan semakin rendah.
Jawaban: A
(3). NaCl dan Glukosa Dilarutkan Ke Air Titik Didih Sama
88. Jika 585 gram NaCl (Mr = 58,5) dan 1800 gram glukosa (Mr = 180) dilarutkan ke air dengan volume yang sama maka akan dihasilkan dua macam larutan yang memiliki titik didih yang sama.
SEBAB
Kedua larutan tersebut memiliki molalitas yang sama.
88. Pembahasan:
Jika 585 gram NaCl dan 1800 gram glukosa dilarutkan dalam air dengan volume sama maka akan dihasilkan larutan dengan molalitas sama.

Larutan NaCl mempunyai titik didih lebih tinggi sebab NaCl bersifat elektrolit sehingga dalam larutan menghasilkan jumlah partikel yang lebih besar.
Jawaban: D
(4). Kenaikan Titik Didih Larutan Zat Organik Nonelektrolit Na2SO4
85. Sebanyak 14,2 g Na2SO4(Mr = 142) dilarutkan dalam 500 ml air (ρ = 1 g/ml) mempunyai titik didih 100,3°C. Bila 20 g zat organik nonelektrolit digunakan untuk menggantikan Na2SO4, titik didih larutannya menjadi 100,1°C. Massa molekul relatif zat organik tersebut adalah …
A. 44 B. 67 C. 80 D. 100 E. 200
85. Pembahasan:
Kenaikan titik didih larutan:

Jawaban: B
(5). Ikatan Hidrogen @ Titik Didih Amonia
34. Meskipun berat molekulnya hampir sama, titik didih amonia (NH3) lebih rendah daripada titik didih air (H2O).
SEBAB
Ikatan hidrogen antarmolekul air lebih kuat dibandingkan antar molekul amonia.
34. Pembahasan:
Ikatan hidrogen adalah ikatan yang terjadi antara unsur H dengan unsur yang keelektronegatifannya tinggi (F, O, N).
H➔F (contoh: HF)
H➔O (contoh: H2O, R-OH, R-COOH)
H➔N (contoh: NH3)
Meskipun berat molekulnya hampir sama, titik didih NH3 lebih rendah daripada titik didih H2O sebab ikatan hidrogen yang terjadi antar molekul H2O lebih kuat daripada antar molekul NH3.
Jawaban: A
(6). Titik Didih Larutan K2co3 Massa Molekul Relatif Zat X
86. Sejumlah 18g zat nonelektrolit X yang tidak mudah menguap dilarutkan dalam 100 g air yang memiliki titik didih yang sama dengan larutan K2CO3 0,3 m. Massa molekul relatif zat X adalah …
A. 60 B. 120 C. 180 D. 200 E. 320
86. Pembahasan:
Sifat Koligatif Larutan Elektrolit
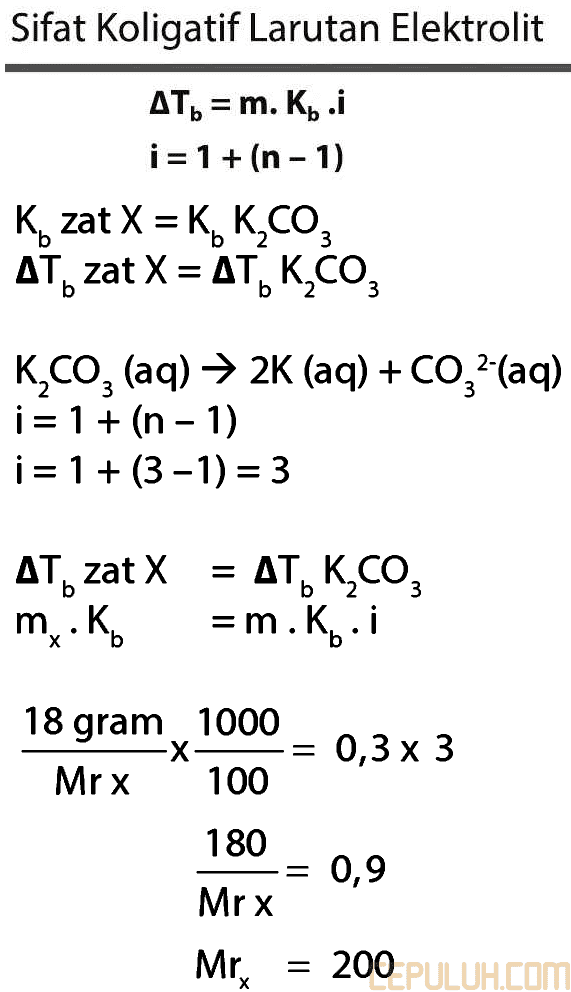
Jawaban: D
(7). Senyawa Titik Didih Tertinggi
87. Jika senyawa-senyawa berikut dilarutkan dalam 500 ml air maka senyawa yang menghasilkan titik didih tertinggi adalah …
A. 7,1 gram Na2SO4(Mr= 142)
B. 11,7 gram NaCl (Mr = 58,5)
C. 18 gram fruktosa (Mr = 180)
D. 36 gram fruktosa (Mr = 180)
E. 68,4 gram fruktosa (Mr = 342)
87. Pembahasan:
Karena volume larutan masing-masing sama maka:

Jawaban: B
(8). Rumus Titik Didih Tertinggi
11. Di antara rumus berikut yang mempunyai titik didih tertinggi adalah …
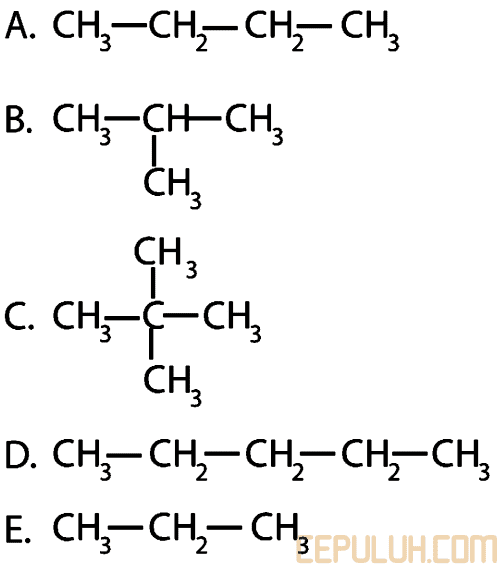
11. Pembahasan:
Semakin banyak jumlah atom karbon, semakin tinggi titik didihnya. A dan ya rantai cabang pada senyawa alkana menurunkan titik didihnya.
| Senyawa alkana dengan Mr yang besar dan rantai yang panjang mempunyai titik didih yang tinggi. |
Jawaban: D
(9). Kenaikan Titik Didih Larutan NaCl
82. Sebanyak 5,85 gram NaCl (Mr = 58,5) dilarutkan dalam 500 gram air (Kb = 0,5), bila diukur pada tekanan 1 atm maka kenaikan titik didih larutan adalah …
A. 0,1°C C. 0,4°C E. 2,0°C
B. 0,2°C D. 1,0°C
82. Pembahasan:
NaCl merupakan larutan elektrolit kuat dengan jumlah ion 2.

Jawaban: B
(10). Kenaikan Titik Didih Larutan Aluminium Klorida
84. pada tekanan 1 atm, larutan 13,35 gram aluminium klorida (Mr = 133,5) dalam 260 g air (Kb = 0,52°C/m) akan mendidih pada …
A. 99,2°C B. 100,2°C C. 100,8°C D. 102,0°C E. 108,0°C
84. Pembahasan:

Jawaban: B
Sifat Koligatif # Larutan Elektrolit
Struktur Atom, Sistem Periodik Unsur # Nama Senyawa
Skala Suhu Termometer Celsius Fahrenheit Reamur
Sifat Koligatif # Titik Didih