(1). Jumlah Partikel Zat Terlarut Dalam Mol Pelarut Tekanan Uap Paling Besar
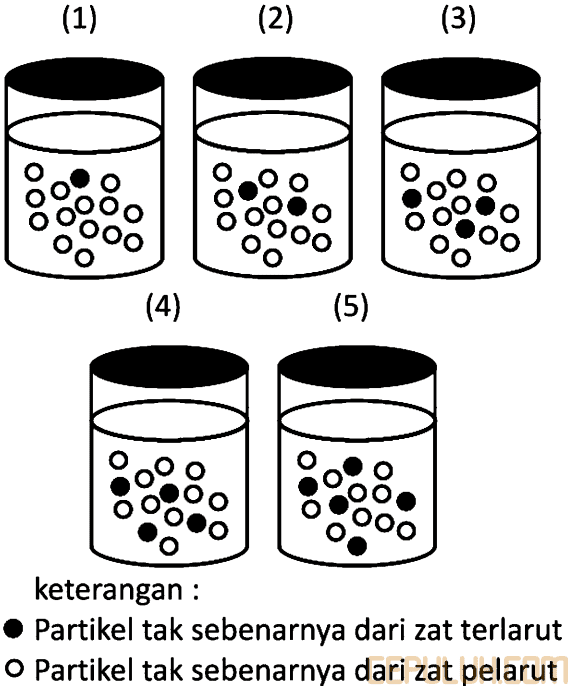
70. Berikut ini jumlah partikel zat terlarut yang terdapat dalam 2 mol pelarut dalam ruangan tertutup.
Berdasarkan gambar tersebut, tekanan uap yang paling besar terdapat pada larutan nomor …
A. 1 B. 2 C. 3 D. 4 E. 5
70. Pembahasan:
Berdasarkan hukum Raoult, P = P°•Xpelarut
■ Semakin besar nilai P maka Xpelarut semakin besar.
■ Psemakin besar jika jumlah partikel zat terlarutnya semakin sedikit dalam jumlah pelarut yang sama.
Gambar 4 menunjukkan jumlah partikel zat terlarut paling sedikit, sehingga tekanan uap larutannya paling besar
Jawaban: D
(2). Partikel Zat Terlarut dan Pelarut Tekanan Uap Paling Kecil
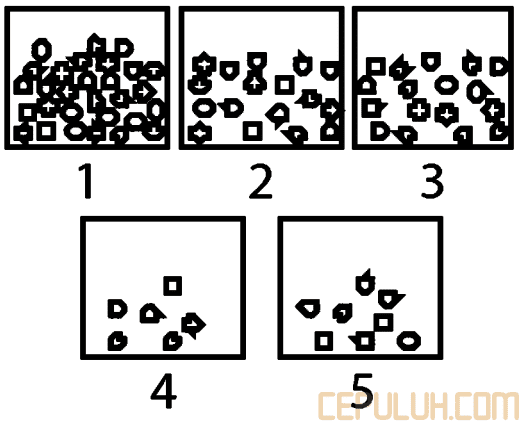
71. Gambar berikut merupakan gambar pertikel zat terlarut dan pelarut yang bukan sebenarnya.
Tekanan uap larutan paling kecil terdapat pada wadah …
A. 1 B. 2 C. 3 D. 4 E. 5
71. Pembahasan:
P = Xpelarut• P°
Tekanan uap paling kecil (P kecil) apabila nilai Xpelarut kecil, hal ini berarti P kecil terdapat pada larutan yang mempunyai partikel zat pelarutnya paling sedikit yaitu larutan nomor 1.
Jawaban: A
(3). Partikel Zat Terlarut dan Pelarut Tekanan Uap Paling Kecil
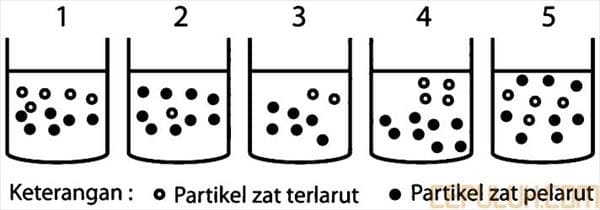
72. Perhatikan gambar berikut!
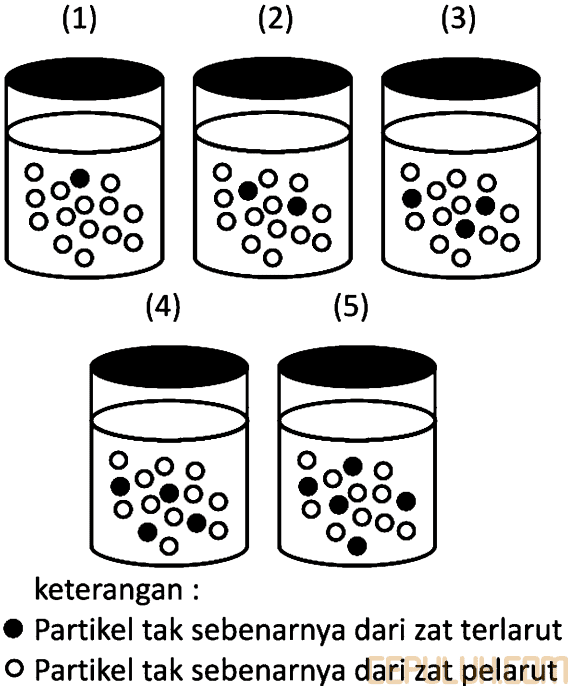
keterangan :
• Partikel tak sebenarnya dari zat terlarut
o Partikel tak sebenarnya dari zat pelarut
Larutan yang mempunyai tekanan uap paling kecil terdapat pada gambar nomor …
A. (1) B. (2) C. (3) D. (4) E. (5)
72. Pembahasan:
Larutan yang mempunyai tekanan uap paling kecil terdapat pada gambar nomor (5).
Jawaban: E
(4). Penurunan Tekanan Tekanan Jenuh Uap Air Molalitas Larutan Sukrosa
68. Larutan sukrosa dalam air memiliki penurunan tekanan sebesar ⅙P° mmHg, di mana P° adalah 6 tekanan jenuh uap air. Molalitas larutan sukrosa adalah … (Mr sukrosa = 342,air = 18)
A. 0,83 m B. 5,55 m C. 9,26 m D. 11,1m E. 22,2 m
68. Pembahasan:
Penurunan tekanan uap larutan dapat dihitung dengan rumus:

Jawaban: D
(5). Larutan Tekanan Uap Jenuh Massa Molekul Relatif Mr Zat X
73. Zat X sebanyak 15 gram dilarutkan dalam 90 gram air. Larutan ini mempunyai tekanan uap jenuh 28,85 mmHg. pada suhu yang sama, air mempunyai tekanan uap jenuh 30 mmHg. Massa molekul relatif (Mr) zat X adalah …
A. 30 B. 60 C. 75 D. 90 E. 150
73. Pembahasan:
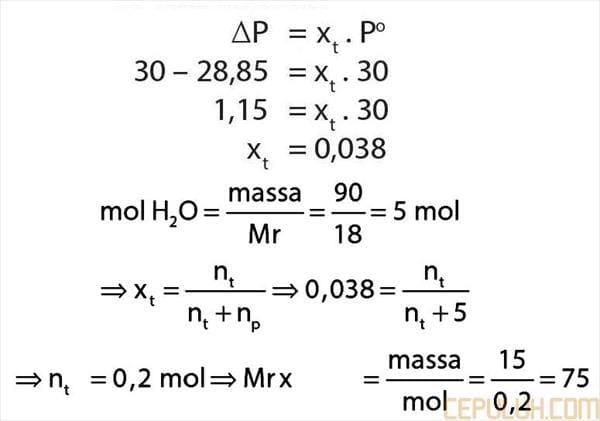
Jawaban: C
(6). Tekanan Uap Total Larutan
69. pada temperatur 20°C, sikloheksana dan toluena mempunyai tekanan uap murni masing-masing sebesar 70 torr dan 20 torr. Tekanan uap total larutan yang terdiri atas 50% mol sikloheksana dan 50% mol toluena adalah … torr
A. 20 B. 45 C. 50 D. 70 E. 100
69. Pembahasan:
Tekanan uap total larutan
= 50%•P sikloheksana + 50%•P toluena
= 50%•70 + 50%•20 = 45 torr.
Jawaban: B
Sifat Koligatif # Titik Beku
Sifat Koligatif # Titik Didih
Sifat Koligatif # Larutan Elektrolit