(1). Larutan Buffer @ Konstanta Disosiasi Asam
34. Diketahui konstanta disosiasi asam, Ka, untuk beberapa jenis asam sebagai berikut:
| Asam | Konstanta Disosiasi Asam (Ka) |
|---|---|
| H3PO4 | 7×10-3 |
| H2PO4– | 8×10-8 |
| HPO42- | 5×10-13 |
dari informasi tersebut, campuran manakah yang paling baik digunakan untuk membuat larutan buffer dengan nilai pH = 9?
A. NaH2PO4 murni D. H2PO4– + HPO42-
B. H3PO4 + H2PO4– E. HPO42- + PO43-
C. H2PO4– + PO43-
34. Pembahasan:
pH larutan buffer = 9
[H+] = 10-9
Maka yang paling baik digunakan asam dengan Ka
≈ 10-9( H2PO4–) dengan basa konjugasinya (HPO42-).
Jawaban: D
(2). pH Asam Basa Lemah Tetapan Ionisasi
Warna larutan asam format 0,1 M (dengan volume tertentu) yang diberi dua tetes indikator adalah sama dengan warna larutan asam klorida 2.10-3 M (dengan volume yang sama) yang diberi juga dua tetes indikator tersebut. dapat disimpulkan bahwa tetapan ionisasi asam format tersebut adalah ….
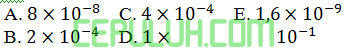
Jawab: C Pembahasan:
Warna larutan menjadi sama artinya pH sudah sama.
Asam:
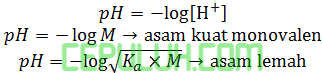
Asam klorida HCl→H++Cl– adalah monovalen melepas satu ion H+ dalam air.
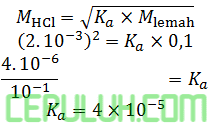
(3). pH Asam Basa Lemah Tetapan Ionisasi
pH dari 100 ml larutan HCN 0,1 M adalah 4 maka pH dari 50 ml larutan HCN 0,04M adalah ….
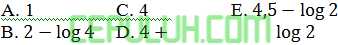
Jawab: E Pembahasan:
Ini bukan pengenceran. Jika konsentrasi sudah diketahui maka volume tidak diperlukan untuk menghitung [H+].
Asam sianida HCN adalah asam lemah.
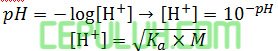
Diketahui:
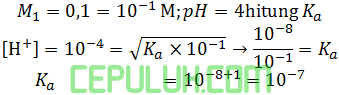
Diketahui:
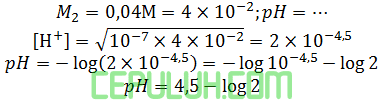
(4). pH Asam Basa Lemah Tetapan Ionisasi
Larutan asam asetat (Ka=10-5) mempunyai pH yang sama dengan larutan 2.10-3 M asam klorida. Konsentrasi asam asetat ini ….M.
Jawaban: C Pembahasan:
Asam:
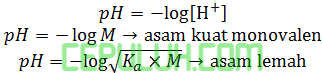
Asam klorida HCl→H++Cl– adalah monovalen melepas satu ion H+ dalam air.
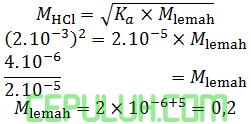
(5). pH Asam Basa Lemah Tetapan Ionisasi
Derajat ionisasi asam format adalah 0,01. jika tetapan ionisasinya 1,8×10-4 maka pH larutan itu adalah ….
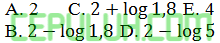
Jawaban: B Pembahasan:
Asam karboksilat termasuk asam lemah di antaranya asam format HCOOH dan asam asetat.
Diketahui α=0,01=10-2; Ka=1,8×10-4 hitung konsentrasi.
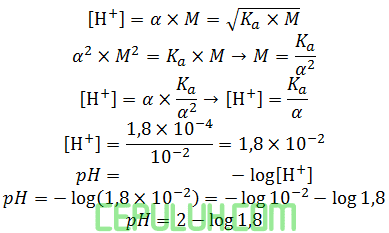
(6). pH Asam Basa Lemah Tetapan Ionisasi
pH dari 100 ml larutan CH3COOH 0,4 M jika diketahui Ka=10-5 adalah ….
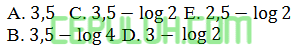
Jawab: D Pembahasan:
Jika konsentrasi sudah diketahui maka volume tidak diperlukan untuk menghitung [H+].
Asam asetat CH3COOH adalah asam lemah.
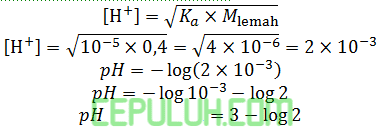
(7). pH Asam Basa Lemah Tetapan Ionisasi
Sebanyak 10 ml larutan asam asetat (Ka=10-5) dengan pH=3 dicampurkan dengan 90 ml air, maka pH larutan asam asetat setelah ditambah air adalah ….
Jawaban: D Pembahasan:
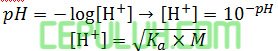
Diketahui:
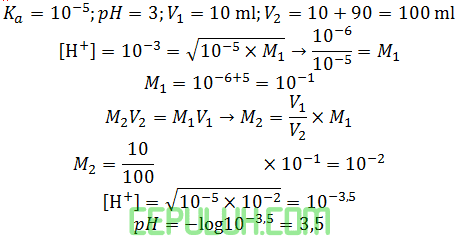
(8). pH Asam Basa Lemah Tetapan Ionisasi
ion H3 yang terdapat dalam larutan CH3COOH 0,1M(Ka=1,96×10-5) adalah ….M.
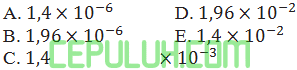
Jawab: C Pembahasan:
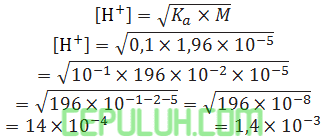
(9). Tetapan Suatu Asam Ha Maka pH Larutan Ha
2. Jika tetapan suatu asam HA adalah 10-5 maka pH larutan HA 0,1 M adalah …
A. 5 B. 4 C. 3 D. 2 E. 1
2. Pembahasan:
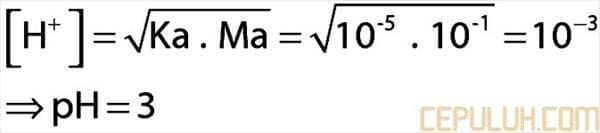
Jawaban: C
(10). Larutan Asam Lemah Ha pH Pka
26. Suatu larutan asam lemah HA 1,0×10-2 M mempunyai pH = 4,0. Nilai pKa asam HA tersebut adalah …
A. 4,9 B. 6,0 C. 7,0 D. 8,0 E. 10,0
26. Pembahasan:
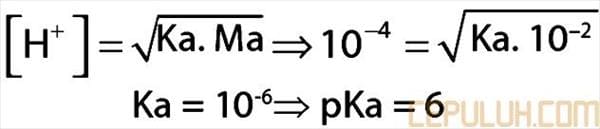
Jawaban: B
Larutan Asam-Basa # Arrhenius
Larutan Asam-Basa # pH pOH Sisa Kuat
Larutan Asam-Basa # Warna Indikator Trayek pH
Larutan Asam-Basa # Titrasi Asam Basa
Larutan Asam-Basa # Bronsted Lowry Konjugasi Donor Akseptor
Derajat Ionisasi Asam Ka