(1). Kecepatan Reaksi Konsentrasi A Dijadikan 2 Kali Semula
20. untuk reaksi A(g) + B(g) ➔ C(g) bila konsentrasi A dijadikan 2 kali semula, ternyata kecepatan reaksinya juga menjadi 2 kali semula. Bila konsentrasi B dijadikan 2 kali semula, ternyata kecepatan reaksinya menjadi 4 kali semula maka dapat dinyatakan …
A. Kecepatan reaksi = k [A]·[B]
B. Kecepatan reaksi = k [A]·[B]2
C. Kecepatan reaksi = k [A]2·[B]2
D. Kecepatan reaksi = k [A]2·[B]4
E. Kecepatan reaksi = k [A]·[B]4
20. Pembahasan:
Orde reaksi A (persamaan 1 dan 2):
Orde reaksi B (persamaan 1 dan 3):
Jadi, persamaan kecepatan reaksinya adalah:

Jawaban: B
(2). Kecepatan Reaksi Menjadi Kali untuk Setiap Kenaikan Suhu
30. Kecepatan reaksi pada saat tertentu menjadi 2 kali untuk setiap kenaikan suhu 10°C. Berapa kali kecepatan reaksi tersebut akan berlangsung pada suhu 30°C?
A. 2 B. 8 C. 16 D. 32 E. 64
30. Pembahasan:
Kecepatan reaksi pada suhu 50°C:
Kecepatan reaksi pada suhu 20°C:

Laju reaksi pada suhu 50°C adalah 8 kali lebih cepat dari laju reaksi pada suhu 20°C.
Jawaban: B
(3). Reaksi Akan Berlangsung Tiga Kali Lebih Cepat dari Semula Setiap Kenaikan Suhu
1. Reaksi akan berlangsung tiga kali lebih cepat dari semula setiap kenaikan 20°C. Jika pada suhu 30°C suatu berlangsung 3 menit maka pada suhu 70°C reaksi akan berlangsung selama … menit
A. ⅓ B. ⅔ C. 1 D. 4 E. 12
1. Pembahasan:
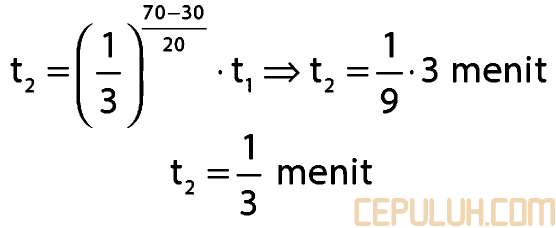
Jawaban: A
(4). Volume Gas Diperkecil Kali Semula Maka Kecepatan Reaksi Kali Semula
27. Kecepatan reaksi dari suatu reaksi gas dinyatakan sebagai v = k [A]·[B]. Bila volume yang ditempati gas-gas tersebut tiba-tiba diperkecil ¼ kali volume semula maka kecepatan reaksinya … kali kecepatan reaksi semula.
A. ⅛ B. 1/16 C. 4 D. 8 E. 16
27. Pembahasan:
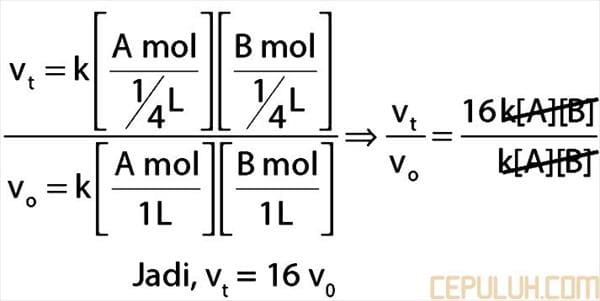
Jawaban: E
(5). Volume Sistem Tiba-Tiba Diperbesar Kali Volume Semula Maka Laju Reaksi
21. Rumus laju reaksi suatu gas dinyatakan sebagai v = k [A]·[B]2. Bila volume sistem tiba-tiba diperbesar 4 kali volume semula maka laju reaksinya … kali laju reaksi semula.
A. 1/16 B. 1/64 C. 4 D. 16 E. 64
21. Pembahasan:
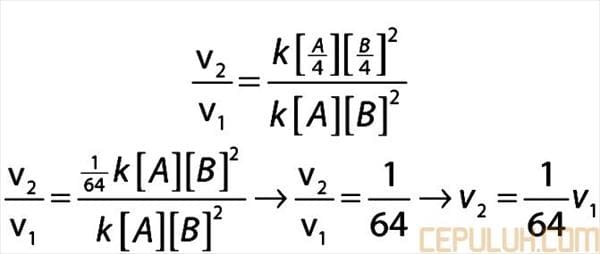
Jawaban: B
(6). Faktor yang Mempengaruhi Laju Reaksi
dari reaksi A+B→zat hasil
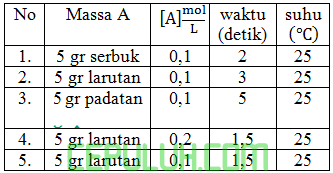
dari percobaan 1 dan 3 laju reaksi dipengaruhi oleh ….
A. konsentrasi D. sifat zat
B. suhu E. luas permukaan
C. Katalis
Jawaban: E pembahasan:
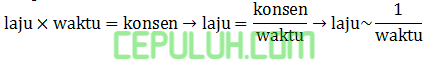
waktu berbanding terbalik dari laju. Waktu reaksi 1 dan 3 dipengaruhi perbedaan:
∎ jumlah luas permukaan seluruh partikel paling banyak, larutan, serbuk, padataan.
(7). Faktor yang Mempengaruhi Laju Reaksi
Soal Pembahasan 1 Faktor yang Mempengaruhi Laju Reaksi
Reaksi manakah yang berlangsung dengan laju paling cepat ….
A. CaCO3 serbuk dengan HCl 0,01M
B. CaCO3 butiran dengan HCl 0,01M
C. CaCO3 serbuk dengan HCl 0,02M
D. CaCO3 butiran dengan HCl 0,02M
Jawab: C Pembahasan:
Laju reaksi paling cepat jika
∎ jumlah luas permukaan seluruh partikel paling banyak, sejumlah serbuk lebih cepat habis bereaksi dari pada butiran.
∎ konsentrasi paling besar (M).
Di antara opsi laju reaksi (CaCO3 serbuk dengan HCl 0,02M) paling cepat.
(8). Faktor yang Mempengaruhi Laju Reaksi
Diketahui data hasil sebagai berikut:
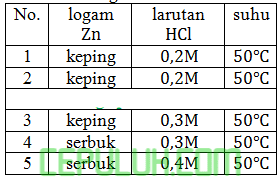
Reaksi antara logam Zn dan larutan HCl yang berlangsung paling cepat adalah ….
A. 1 B. 2 C. 3 D. 4 E. 5
Jawab: E Pembahasan:
Laju reaksi paling cepat jika:
∎ jumlah luas permukaan seluruh partikel paling banyak, sejumlah serbuk lebih banyak jumlah luas dari sebuah lempeng.
∎ konsentrasi (M) paling banyak.
∎ suhu paling tinggi.
Jadi nomor 5 paling cepat.
(9). Kecepatan Reaksi Setiap Kenaikan Suhu
28. Reaksi A + B ➔ C + D, pada suhu 25°C berlangsung sempurna dalam waktu 12 menit. Apabila setiap kenaikan suhu 10°C kecepatan reaaksinya menjadi 2 kali semula maka pada suhu 55°C reaksi akan berlangsung sempurna dalam … menit
A. 0,5 B. 1 C. 1,5 D. 2 E. 2,5
28. Pembahasan:
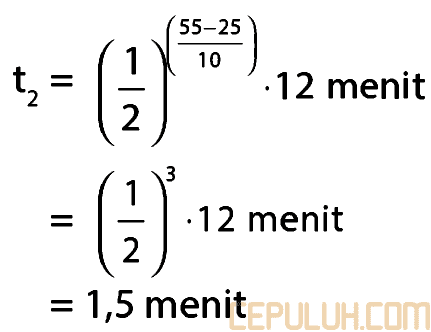
Jawaban: C
(10). Faktor yang Mempengaruhi Laju Reaksi
Data percobaan untuk reaksi A+B→C
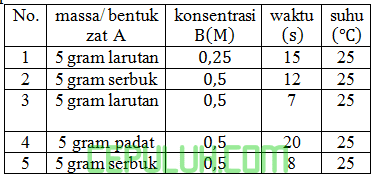
pada percobaan (2) dan (5) faktor yang mempengaruhi laju adalah ….
A. waktu D.bentuk
B.konsentrasi E. katalis
C. suhu
Jawab: E Pembahasan:
Waktu berkebalikan dari laju reaksi. Waktu reaksi pada percobaan (2) dan (5) dipengaruhi perbedaan atau pemakaian katalis karena massa, bentuk, konsentrasi dan suhu sama, tetapi waktu reaksi berbeda.
Laju Reaksi # Konstanta Tetapan
Laju Reaksi # Orde Total Tingkat
Laju Reaksi # Lama Waktu Reaksi
Rumus Persamaan Laju Reaksi
Laju Reaksi # Laju Kecepatan
Laju Reaksi # Faktor Kali Perubahan Suhu Volume