(1). Larutan AgNO3 KSP Garam yang Akan Larut
58. Sebanyak 200 ml larutan AgNO3 0,02 M, masing-masing dimasukkan ke dalam 5 wadah yang berisi 5 jenis larutan yang mengandung ion S2-, PO43-, CrO42-, Br–, dan SO42- dengan volume dan molaritas yang sama.
Jika harga KSP:
Ag2S = 2×10-49
Ag2PO4 =1×10-20
Ag2CrO4 =6×10-5
Ag2Br = 5×10-13
Ag2SO4 = 3×10-5
Maka garam yang akan larut adalah …
A. Ag2S dan Ag3PO4 D. Ag3PO4 dan AgBr
B. Ag2S dan AgBr E. AgBr dan AgSO4
C. Ag2CrO4 dan Ag2SO4
58. Pembahasan:
Qc > KSP artinya terbentuk endapan
Qc = KSP artinya mulai terbentuk endapan
Qc < KSP artinya belum terbentuk endapan
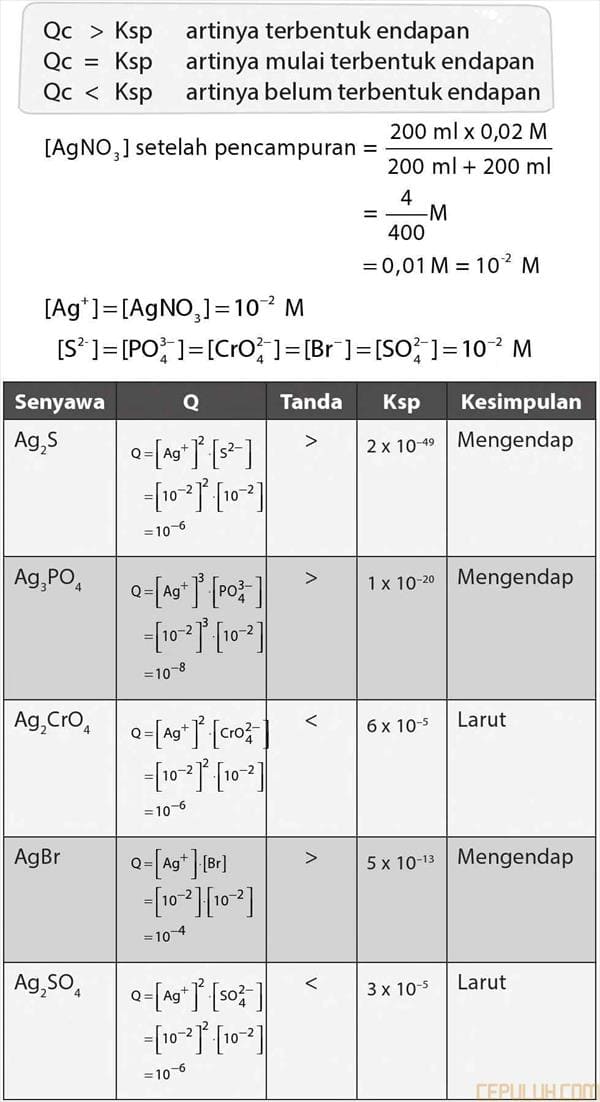
Jawaban: C
(2). NaOH CH3COOH Ditetesi Larutan Encer CaCl2 Tepat Jenuh Mengendap Ca(OH)2
59. 100 ml NaOH 0,008 M + 100 ml CH3COOH 0,008 M ke dalam larutan reaksi ditetesi larutan encer CaCl2 dan penetesan diakhiri ketika larutan tepat jenuh tepat akan mengendap Ca(OH)2. Jika Kw = 10-14,
KSP Ca(OH)2 = 4×10-16, Ka = 10-5 maka [Ca2+] pada saat tepat jenuh adalah …
A. 10-1M D. 10-4M
B. 10-2M E. 10-5M
C. 10-3M
59. Pembahasan:

Jawaban: D
(3). paling sedikit MgCl2 agar diperoleh larutan yang jenuh
10. Agar diperoleh larutan yang jenuh, paling sedikit MgCl2 yang harus ditambahkan ke dalam satu liter larutan NaOH dengan pH=12 adalah … mol. (Ksp Mg(OH)2=1,5×10-11 )
Jawab: A
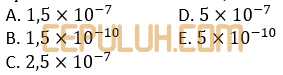
Larutan jenuh atau endapan hampir terbentuk saat Qc=Ksp. Anggap MgCl2 berupa padatan dan volumenya diabaikan sehingga tidak ada perubahan volume campuran.
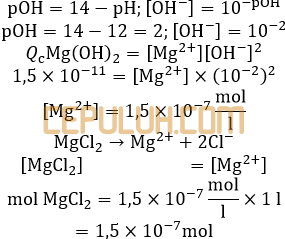
(4). Diket Ksp LSO4=2,5.10-5 ditanya massa relatif
5. Suatu garam LSO4 memiliki Ksp LSO4=2,5.10-5. Jika 0,34 gram garam tersebut terdapat dalam 500 ml larutan jenuhnya, besarnya massa molekul relatif LSO4 adalah ….
A. 34 B. 68 C. 136 D. 272 E. 544
Jawab: C Bahas:
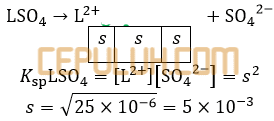
Menghitung kelarutan seperti menghitung konsentrasi.
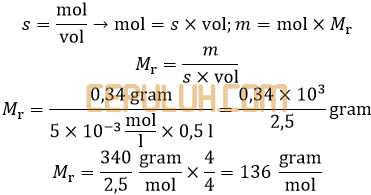
(5). Paling sedikit berapa mol MgCl2
8. Paling sedikit berapa mol MgCl2 yang harus ditambahkan kedalam larutan NaOH dengan pH=12 agar diperoleh larutan yang jenuh dengan Mg(OH)2 jika Ksp Mg(OH)2=10-11 ….
Jawab: D Bahas:
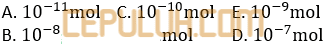
NaOH salah satu basa. Supaya larutan jenuh atau hampir muncul endapan maka
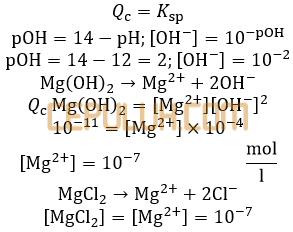
(6). Kapan Larutan Tepat Jenuh?
Larutan tepat jenuh berarti penambahan zat yang sama tidak bisa larut sehingga mulai terjadi endapan. Itu terjadi saat hasil kali ion penyusunnya sama dengan hasil kali kelarutan. Misalkan pencampuran XY dan AB menyusun XB dimana
AB→A++B–
Qc=Ksp
[X+ ][B– ]=Ksp XB
Jika Qc < Ksp maka penambahan zat masih bisa larut. Jika Qc > Ksp maka penambahan zat masih tidak bisa larut atau terjadi endapan.
(7). Diket Ksp CaSO4=4×10-8 ditanya massa
2. Diketahui Ksp CaSO4=4×10-8 maka banyaknya CaSO4 (Mrp=136) yang larut dalam 250 cm3 larutan adalah ….mg (mini gram).
A. 1,36 C. 2,72 E. 27,20
B. 2,17 D. 6,80
Jawab: D pembahasan:
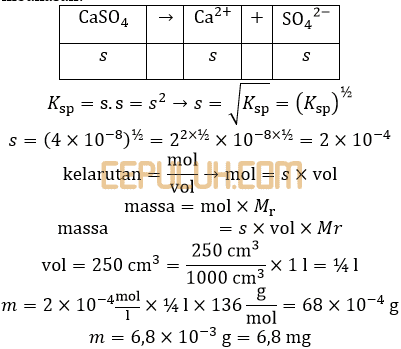
(8). Diket Ksp PbI2=4.10-9 ditanya massa
4. pada suhu Ksp PbI2=4.10-9, maka PbI2 yang dapat larut dalam 100 ml air pada suhu sebanyak ….(Mrp PbI2=462)
A. 0,462 mg C. 462 mg E. 92,4 mg
B. 4,62 mg D. 46,2 mg
Jawab: D Bahas:
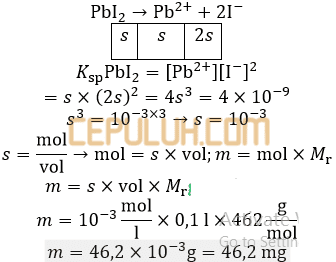
(9). Diket kelarutan Mg(OH)2 ditanya massa
1. Jika Ksp Mg(OH)2=4×10-12 maka kelarutan Mg(OH)2 (Mr=58 g/mol) dalam 100 ml larutan adalah … gram.
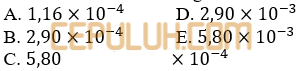
Jawab: C pembahasan:

(10). Diket Ksp Ca(OH)2=4×10-6 ditanya massa
3. Jika Ksp Ca(OH)2=4×10-6, (Mrp Ca(OH)2=74) massa paling banyak Ca(OH)2 yang dapat larut dalam 250 ml air adalah … gram.
A. 7,400 C. 0,740 E. 0,185
B. 3,700 D. 0,370
Jawab: E Bahas:
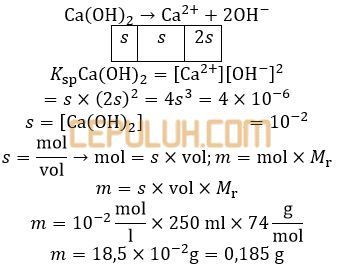
Kelarutan KSP # pH Asam Basa
Kelarutan KSP Endapan
Kelarutan KSP # Hasil Kali Kelarutan KSP
Massa Jenuh Terlarut