(1). Soal Bentuk Molekul Senyawa Ion AlCl4- Tetrahedral
Soal bentuk molekul ion AlCl4– (nomor atom Al=13, elektron valensi atom Al=3; nomor atom Cl=17, elektron valensi atom Cl=7)
Jawaban: berbentuk tetrahedral sesuai AX4.
Pembahasan:
Konfigurasi elektron atom Al: 1s2 2s2 2p6 3s2 3p1, elektron valensi 3.
Konfigurasi elektron ion Al–: 1s2 2s2 2p6 3s2 3p2, elektron valensi 4.
Konfigurasi elektron atom Cl: 1s2 2s2 2p6 3s2 3p5, elektron valensi 7.
Bentuk molekul senyawa AlCl4– menurut teori VSEPR
Struktur Lewis:
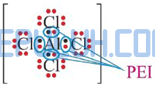
Al– sebagai pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom Cl di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka ion Al– tidak memiliki pasangan elektron bebas (PEB=0) sehingga AlCl4– diprediksi berbentuk tetrahedral AX4.
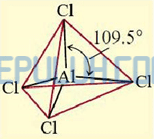
Bentuk molekul senyawa AlCl4– menurut teori hibridisasi
Diagram orbital ion Al–:
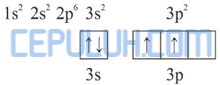
Dalam molekul AlCl4–, Al– mengikat 4 atom Cl. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 3s ke orbital 3p.
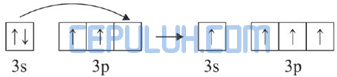
Kemudian 4 elektron dari 4 atom Cl memasuki orbital 3s dan 3p sehingga terbentuk orbital hibrida sp3.
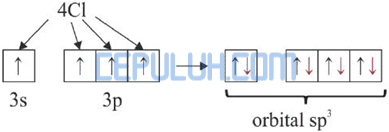
Jadi, molekul AlCl4– diprediksi berbentuk tetrahedral.
(2). Bentuk Molekul Ion AlCl4- Tetrahedral
AlCl4– (nomor atom Al=13, elektron valensi atom Al=3; nomor atom Cl=17, elektron valensi atom Cl=7)
Jawaban: berbentuk tetrahedral sesuai AX4.
Pembahasan:
Konfigurasi elektron atom Al: 1s2 2s2 2p6 3s2 3p1, elektron valensi 3.
Konfigurasi elektron ion Al–: 1s2 2s2 2p6 3s2 3p2, elektron valensi 4.
Konfigurasi elektron atom Cl: 1s2 2s2 2p6 3s2 3p5, elektron valensi 7.
Bentuk molekul senyawa AlCl4– menurut teori VSEPR
Struktur Lewis:
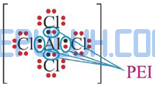
Al– sebagai pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom Cl di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka ion Al– tidak memiliki pasangan elektron bebas (PEB=0) sehingga AlCl4– diprediksi berbentuk tetrahedral AX4.
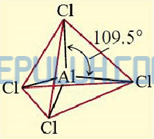
Bentuk molekul senyawa AlCl4– menurut teori hibridisasi
Diagram orbital ion Al–:
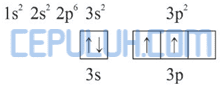
Dalam molekul AlCl4–, Al– mengikat 4 atom Cl. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 3s ke orbital 3p.
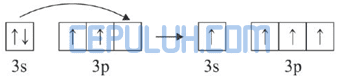
Kemudian 4 elektron dari 4 atom Cl memasuki orbital 3s dan 3p sehingga terbentuk orbital hibrida sp3.
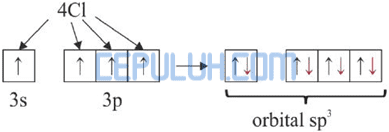
Jadi, molekul AlCl4– diprediksi berbentuk tetrahedral.
(3). Soal Bentuk Molekul Hibridisasi Senyawa SnCl4 Tetrahedral
Soal bentuk molekul senyawa SnCl4 (nomor atom Sn=50, elektron valensi atom Sn=4; nomor atom Cl=17, elektron valensi atom Cl=7)
Jawaban: tetrahedral AX4.
Pembahasan:
Konfigurasi elektron atom Sn: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p2, elektron valensi 4.
Konfigurasi elektron atom Cl: 1s2 2s2 2p6 3s2 3p5, elektron valensi 7.
Bentuk molekul senyawa SnCl4 menurut teori VSEPR
Struktur Lewis:

Atom Sn sebagai atom pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom Cl di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka atom Sn tidak memiliki pasangan elektron bebas (PEB=0) sehingga SnCl4 diprediksi berbentuk tetrahedral sesuai AX4.
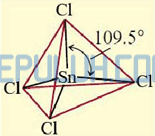
Bentuk molekul senyawa SnCl4 menurut teori hibridisasi
Diagram orbital atom Sn:

Dalam molekul SnCl4, satu atom Sn mengikat 4 atom Cl. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 5s ke 5p.
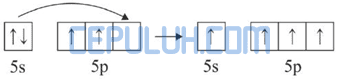
Kemudian 4 elektron dari 4 atom Cl memasuki orbital 5s dan 5p sehingga terbentuk orbital hibrida sp3.
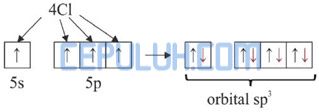
Jadi, molekul SnCl4 diprediksi berbentuk tetrahedral.
(4). Soal Bentuk Molekul Senyawa Ion NH4+ Tetrahedral
Soal bentuk molekul ion NH4+ (nomor atom N=7, elektron valensi atom N=5; nomor atom H=1, elektron valensi atom H=1)
Jawaban: berbentuk tetrahedral sesuai AX4.
Pembahasan:
Konfigurasi elektron atom N: 1s2 2s2 2p3, elektron valensi 5.
Konfigurasi elektron ion N+: 1s2 2s2 2p2, elektron valensi 4.
Konfigurasi elektron atom H: 1s1, elektron valensi 1.
Bentuk molekul senyawa NH4+ menurut teori VSEPR
Struktur Lewis:
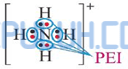
N+ sebagai pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom H di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka ion N+ tidak memiliki pasangan elektron bebas (PEB=0) sehingga NH4+ diprediksi berbentuk tetrahedral AX4.
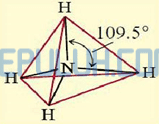
Bentuk molekul senyawa NH4+ menurut teori hibridisasi
Diagram orbital ion N+:
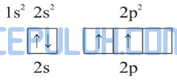
Dalam molekul NH4+, N+ mengikat 4 atom H. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 2s ke orbital 2p.
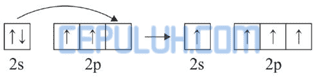
Kemudian 4 elektron dari 4 atom H memasuki orbital 2s dan 2p sehingga terbentuk orbital hibrida sp3.
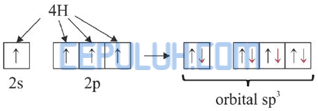
Jadi, molekul NH4+ diprediksi berbentuk tetrahedral.
(5). Bentuk Molekul Ion NH4+ Tetrahedral
Soal bentuk molekul senyawa NH4+ (nomor atom N=7, elektron valensi atom N=5; nomor atom H=1, elektron valensi atom H=1)
Jawaban: berbentuk tetrahedral sesuai AX4.
Pembahasan:
Konfigurasi elektron atom N: 1s2 2s2 2p3, elektron valensi 5.
Konfigurasi elektron ion N+: 1s2 2s2 2p2, elektron valensi 4.
Konfigurasi elektron atom H: 1s1, elektron valensi 1.
Bentuk molekul senyawa NH4+ menurut teori VSEPR
Struktur Lewis:
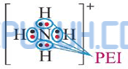
N+ sebagai pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom H di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka ion N+ tidak memiliki pasangan elektron bebas (PEB=0) sehingga NH4+ diprediksi berbentuk tetrahedral AX4.
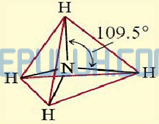
Bentuk molekul senyawa NH4+ menurut teori hibridisasi
Diagram orbital ion N+:
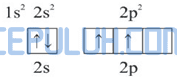
Dalam molekul NH4+, N+ mengikat 4 atom H. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 2s ke orbital 2p.
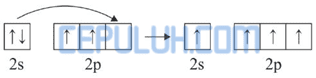
Kemudian 4 elektron dari 4 atom H memasuki orbital 2s dan 2p sehingga terbentuk orbital hibrida sp3.
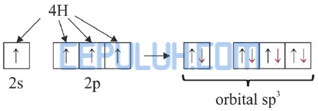
Jadi, molekul NH4+ diprediksi berbentuk tetrahedral.
(6). Soal Bentuk Molekul Senyawa SiBr4 Tetrahedral
Soal bentuk molekul senyawa SiBr4 (nomor atom Si=14, elektron valensi atom Si=4; nomor atom Br=35, elektron valensi atom Br=7)
Jawaban: Tetrahedral AX4.
Pembahasan:
Konfigurasi elektron atom Si: 1s2 2s2 2p6 3s2 3p2, elektron valensi 4.
Konfigurasi elektron atom Br: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5, elektron valensi 7.
Bentuk molekul senyawa SiBr4 menurut teori VSEPR
Struktur Lewis:

Atom Si sebagai atom pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom Br di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka atom Si tidak memiliki pasangan elektron bebas (PEB=0) sehingga SiBr4 diprediksi berbentuk tetrahedral sesuai AX4.
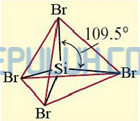
Bentuk molekul senyawa SiBr4 menurut teori hibridisasi
Diagram orbital atom Si:
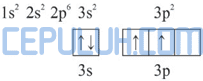
Dalam molekul SiBr4, satu atom Si mengikat 4 atom Br. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 3s ke orbital 3p.
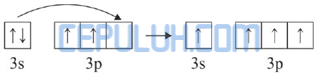
Kemudian 4 elektron dari 4 atom Br memasuki orbital 3s dan 3p sehingga terbentuk orbital hibrida sp3.
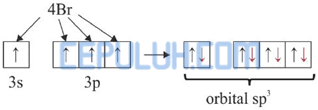
Jadi, molekul SiBr4 diprediksi berbentuk tetrahedral
(7). Soal Bentuk Molekul Senyawa SiCl4 Tetrahedral
Soal bentuk molekul senyawa SiCl4 (nomor atom Si=14, elektron valensi atom Al=4; nomor atom Cl=17, elektron valensi atom Cl=7)
Jawaban: tetrahedral AX4.
Pembahasan:
Konfigurasi elektron atom Si: 1s2 2s2 2p6 3s2 3p2, elektron valensi 4.
Konfigurasi elektron atom Cl: 1s2 2s2 2p6 3s2 3p5, elektron valensi 7.
Bentuk molekul senyawa SiCl4 menurut teori VSEPR
Struktur Lewis:

Atom Si sebagai atom pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom Cl di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka atom Si tidak memiliki pasangan elektron bebas (PEB=0) sehingga SiCl4 diprediksi berbentuk tetrahedral sesuai AX4.
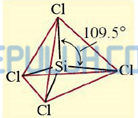
Bentuk molekul senyawa SiCl4 menurut teori hibridisasi
Diagram orbital atom Si:
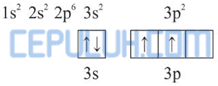
Dalam molekul SiCl4, satu atom Si mengikat 4 atom Cl. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 3s ke 3p.
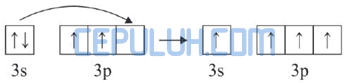
Kemudian 4 elektron dari 4 atom Cl memasuki orbital 3s dan 3p sehingga terbentuk orbital hibrida sp3.
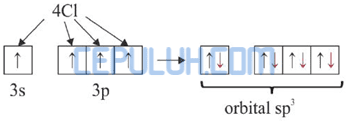
Jadi, molekul SiCl4 diprediksi berbentuk tetrahedral.
(8). Soal Bentuk Molekul Senyawa SiF4 Tetrahedral
Soal bentuk molekul senyawa SiF4 (nomor atom Si=14, elektron valensi atom Al=4; nomor atom Cl=17, elektron valensi atom Cl=7)
Jawaban: tetrahedral AX4.
Pembahasan:
Konfigurasi elektron atom Si: 1s2 2s2 2p6 3s2 3p2, elektron valensi 4.
Konfigurasi elektron atom F: 1s2 2s2 2p5, elektron valensi 7.
Bentuk molekul senyawa SiCl4 menurut teori VSEPR
Struktur Lewis:

Atom Si sebagai atom pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom F di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka atom Si tidak memiliki pasangan elektron bebas (PEB=0) sehingga SiF4 diprediksi berbentuk tetrahedral sesuai AX4.
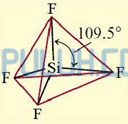
Bentuk molekul senyawa SiF4 menurut teori hibridisasi
Diagram orbital atom Si:
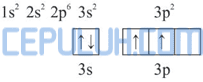
Dalam molekul SiF4, satu atom Si mengikat 4 atom F. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 3s ke 3p.
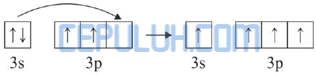
Kemudian 4 elektron dari 4 atom F memasuki orbital 3s dan 3p sehingga terbentuk orbital hibrida sp3.
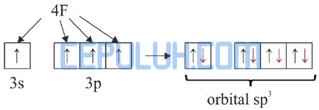
Jadi, molekul SiF4 diprediksi berbentuk tetrahedral.
(9). Soal Bentuk Molekul Hibridisasi Senyawa SiH4 Tetrahedral
Soal bentuk molekul senyawa SiH4 (nomor atom Si=14, elektron valensi atom Si=4; nomor atom H=1, elektron valensi atom H=1)
Jawaban: tetrahedral AX4.
Pembahasan:
Konfigurasi elektron atom Si: 1s2 2s2 2p6 3s2 3p2, elektron valensi 4.
Konfigurasi elektron atom H: 1s1, elektron valensi 1.
Bentuk molekul senyawa SiH4 menurut teori VSEPR
Struktur Lewis:

Atom Si sebagai atom pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom H di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka atom Si tidak memiliki pasangan elektron bebas (PEB=0) sehingga SiH4 diprediksi berbentuk tetrahedral sesuai AX4.
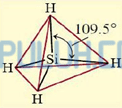
Bentuk molekul senyawa SiH4 menurut teori hibridisasi
Diagram orbital atom Si:
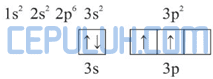
Dalam molekul SiH4, satu atom Si mengikat 4 atom H. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 3s ke 3p.
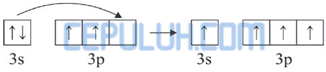
Kemudian 4 elektron dari 4 atom H memasuki orbital 3s dan 3p sehingga terbentuk orbital hibrida sp3.
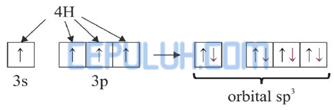
Jadi, molekul SiH4 diprediksi berbentuk tetrahedral.
(10). Soal Bentuk Molekul Senyawa CH4 Tetrahedral
Soal bentuk molekul senyawa CH4 (nomor atom C=6, elektron valensi C=4, nomor atom H=1 elektron valensi atom H=1)
Jawaban: bentuk AX4 adalah tetrahedral
Pembahasan:
konfigurasi elektron atom C: 1s2 2s2 2p2, elektron valensi 4.
konfigurasi elektron atom H: 1s1, elektron valensi 1.
Bentuk molekul senyawa CH4 menurut teori VSEPR.
Struktur Lewis:
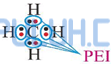
Atom C sebagai atom pusat memiliki 4 elektron valensi, semua elektron valensi terlibat dalam ikatan dengan empat atom H di sekitarnya, masing-masing membentuk ikatan tunggal (PEI=4) maka atom C tidak memiliki pasangan elektron bebas (PEB=0). Sehingga CH4 diprediksi berbentuk tetrahedral AX4.
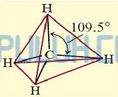
Bentuk molekul senyawa CH4 menurut teori hibridisasi
Diagram orbital atom C:
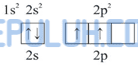
Dalam molekul CH4 satu atom C mengikat 4 atom H. Pengikatan ini dapat berlangsung dengan mengeksitasi 1 elektron dari orbital 2s ke orbital 2p.
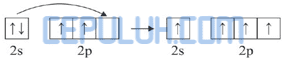
Kemudian, 4 elektron dari 4 atom H memasuki orbital 2s dan 2p sehingga terbentuk orbital hibrida sp2.
Jadi, molekul CH4 diprediksi berbentuk tetrahedral AX4.
Bentuk Molekul Tetrahedral