(1). Jumlah Mol Gas Agar Terjadi Kesetimbangan Kc Tetapan kesetimbangan reaksi

pada suhu 769K adalah 0,05. jika konsentrasi awal PCl5 0,1M, maka pada keadaan setimbang PCl5 yang terurai adalah ….
Jawab: E Pembahasan: Derajat disosiasi adalah pengali mol semula atau rasio mol bereaksi. Perbandingan mol yang bereaksi sama dengan perbandingan koefisien.

Anggap reaksi ini dalam volume 1 liter. Koefisiennya setiap senyawa adalah (1) sebagai pangkat tiap konsentrasi.


Faktorkan persamaan kuadrat ini dengan rumus a,b,c.

Ambil x yang positif:

Persen terurai:

(2). Jumlah Mol Gas Agar Terjadi Kesetimbangan Kc Dalam ruang 1 liter terdapat 1 mol gas HI yang terurai menurut reaksi:

Harga Kc pada saat itu adalah 4, jumlah gas H2 yang ada pada saat setimbang adalah ….mol. A. 0,8 B. 0,6 C. 0,5 D. 0,4 E. 0,2 Jawab: D Pembahasan:

Besar konsentrasi sama dengan mol saat volume 1 liter.

Rumus a,b,c:

Sisa HI 1-x harus (+) maka 1-x > > 0→x < 1 dibaca x kurang dari 1.

(3). Jumlah Mol Gas Agar Terjadi Kesetimbangan Kc Perhatikan reaksi berikut ini:

Bila mula-mula [CO]=0,1mol/L dan [H2O]=0,1mol/L serta Kc=9, maka CO yang berekasi adalah ….mol/L.
Jawab: E Pembahasan: Perbandingan mol yang bereaksi sama dengan perbandingan koefisien.

Koefisiennya setiap senyawa adalah (1) sebagai pangkat tiap konsentrasi.

Faktorkan persamaan kuadrat ini dengan rumus a,b,c.

Ini tidak termasuk karena lebih dari 0,1, mol CO(g) semula.

(4). Menghitung Tetapan Kesetimbangan Kimia Kc Sebanyak 4 mol HI dipanaskan dalam sistem bejana 2 liter pada suhu 120℃, sehingga terurai:

Jika derajat disosiasi dari HI sebesar 0,5 maka harga Kc untuk kesetimbangan diatas adalah ….
Jawab: B Pembahasan: Derajat disosiasi adalah pengali mol semula atau rasio mol bereaksi. Perbandingan mol di baris bereaksi sama dengan perbandingan koefisien.

Konsentrasi senilai mol dibagi volume.

Setiap konsentrasi dipangkatkan koefisien.

(5). Jumlah Mol Gas Agar Terjadi Kesetimbangan Kc Dalam ruang 10 liter dicampur gas N2 dan H2 dengan perbandingan jumlah mol 2∶8. Setelah reaksi terjadi 0,2 mol gas NH3 dan terdapat 0,5 mol H2. Jumlah mol gas N2 dan H2 dalam keadaan setimbang adalah ….

Jawab: A Pembahasan: Tuliskan persamaan reaksi lalu setarakan banyak atom kiri-kanan panah:

Perbandingan mol yang bereaksi sama dengan perbandingan koefisien.

Mol H2(g) semula 8x=0,3+0,5=0,8→x=0,1. Mol N2(g) sisa 2x-0,1=2×0,1-0,1=0,2-0,1=0,1.
(6). Menghitung Tetapan Kesetimbangan Kimia Kc Perhatikan reaksi ini:

Bila 1 mol CO dan 1 mol H2O direaksikan sampai terjadi keseimbangan, dan pada saat tersebut terbentuk 0,2 mol CO2 maka harga tetapan kesetimbangan Kc=⋯

Jawab: A Pembahasan: Perbandingan mol yang bereaksi sama dengan perbandingan koefisien.

Koefisiennya setiap senyawa adalah (1) sebagai pangkat tiap konsentrasi.

(7). Gas Karbon Monoksida dan Hidrogen Membentuk Etanol Harga Tetapan Kesetimbangan Kc
12. Dalam ruangan yang volumenya 3 L direaksikan gas karbon monoksida dan hidrogen membentuk etanol, dengan reaksi kesetimbangan sebagai berikut:
| Mol | CO | H2 | CH3OH |
|---|---|---|---|
| Setimbang | 0,3 | 0,1 | 0,2 |
Harga tetapan kesetimbangan Kc adalah …
A. 1,67·10-3 B. 1,50·10-1 C. 6,67 D. 66,67 E. 600
12. Pembahasan:

Jawaban: C
(8). Menghitung Tetapan Kesetimbangan Kimia Kc HI sebanyak 0,1 mol dimasukkan dalam wadah bervolum 1 liter dan dipanaskan sesuai reaksi:
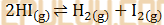
jika terbentuk 0,02 mol gas I2 maka besarnya harga Kc adalah ….

Jawab: C Pembahasan: Perbandingan mol yang bereaksi sama dengan perbandingan koefisien.

Konsentrasi senilai mol karena volume satu liter. Setiap konsentrasi dipangkatkan koefisien.

(9). Menghitung Tetapan Kesetimbangan Kimia Kc Perhatikan reaksi kimia

Bila 1 mol CO dan 1 mol H2O(g) direaksikan sampai terjadi kesetimbangan, dan pada saat tersebut masih tersisa 0,2 mol CO maka harga tetapan keseimbangan Kc adalah ….
Jawab: C Pembahasan: Perbandingan mol di baris bereaksi sama dengan perbandingan koefisien.

Anggap reaksi ini dalam volume 1 liter. Koefisiennya setiap senyawa adalah (1) sebagai pangkat tiap konsentrasi.

(10). Tekanan Total Dalam Sistem adalah P Atm Tetapan Kesetimbangan
9. Perhatikan reaksi kesetimbangan:
2NaHCO3(s) ⇔ Na2CO3(s) + H2O(g) + CO2(g)
Jika natrium hidrogen karbonat dipanaskan dalam ruang hampa pada suhu tertentu. Ternyata dalam kesetimbangan, tekanan total dalam sistem adalah p atm. Tetapan kesetimbangan Kp bagi reaksi ini adalah …
A. Kp = p D. Kp = p2
B. Kp = 2p E. Kp = ½p2
C. Kp = ¼p2
9. Pembahasan:

Jawaban: C
Embed the link of this post
Buka di App!
Kesetimbangan Kimia: Tetapan Kesetimbangan KC KP
Kesetimbangan Kimia: Tetapan Kesetimbangan KC KP